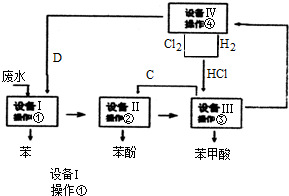
5.下列反应产物属于不饱和烃的是( )
| A. | 苯与氢气的加成反应产物 | B. | 乙醇的消去反应产物 | ||
| C. | 甲烷与氯气的取代反应产物 | D. | 丙烯的加聚反应产物 |
3.配制浓度为2mol•L-1的NaOH100mL,用托盘天平称取NaOH固体时,天平读数将( )
| A. | 等于8.0g | B. | 等于8.00g | C. | 大于8.0g | D. | 等于0.2g |
1. 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | 反应的化学方程式为:N?2M | |
| B. | t2时,正逆反应速率相等,达到平衡 | |
| C. | t3时,正反应速率等于逆反应速率 | |
| D. | t3后,若升高温度则反应速率不一定增大 |
20.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,不正确的是( )
| A. | 加热饱和三氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O$\stackrel{△}{?}$Fe(OH)3(胶体)+3H+ | |
| B. | 硫氢根离子的电离方程式:HS-+H2O?H3O++S2- | |
| C. | 少量氢氧化钙溶液与碳酸氢钠溶液混合的离子方程式:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 0.5mol•L-1的K2Cr2O7溶液中存在如下平衡:Cr2O72-+H2O?2CrO42-+2H+,其平衡常数K的表达式为K=$\frac{{c}^{2}(Cr{{O}_{4}}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{{O}_{7}}^{2-})}$ |
19.下列装置是在制备氨气过程中所用到的装置,正确的是( )
| A. | 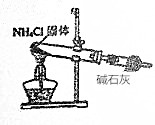 | B. |  | ||
| C. | 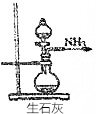 | D. |  |
17.下表列出了A-H八种短周期元素的原子半径和主要化合价.
已知B、E、F与C同周期,回答下列问题:
(1)G在元素周期表中的位置是第三周期VIA族(填周期和族)
(2)上述八种元素中,最高价氧化物的水化物酸性最强的是HClO4(填化学式),气态氢化物水溶液pH>7的是NH3(填化学式);
(3)B、D、E、F四种元素的离子,其离子半径最大的是O2-(填离子符号);
(4)A2D的电子式是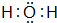 ,B、H两种元素形成化合物的电子式是
,B、H两种元素形成化合物的电子式是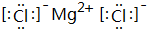 ;
;
(5)A、C、H三种元素组成的化合物的化学式是NH4Cl,该化合物属于离子化合物(填“离子”或“共价”);
(6)E、F两种元素的最高价氧化物的水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
0 155426 155434 155440 155444 155450 155452 155456 155462 155464 155470 155476 155480 155482 155486 155492 155494 155500 155504 155506 155510 155512 155516 155518 155520 155521 155522 155524 155525 155526 155528 155530 155534 155536 155540 155542 155546 155552 155554 155560 155564 155566 155570 155576 155582 155584 155590 155594 155596 155602 155606 155612 155620 203614
| 元素代号 | A | B | C | D | E | F | G | H |
| 原子半径/pm | 37 | 160 | 70 | 66 | 186 | 143 | 104 | 99 |
| 最高化合价 | +1 | +2 | +5 | +1 | +3 | +6 | +7 | |
| 最低化合价 | -3 | -2 | -2 | -1 |
(1)G在元素周期表中的位置是第三周期VIA族(填周期和族)
(2)上述八种元素中,最高价氧化物的水化物酸性最强的是HClO4(填化学式),气态氢化物水溶液pH>7的是NH3(填化学式);
(3)B、D、E、F四种元素的离子,其离子半径最大的是O2-(填离子符号);
(4)A2D的电子式是
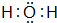 ,B、H两种元素形成化合物的电子式是
,B、H两种元素形成化合物的电子式是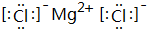 ;
;(5)A、C、H三种元素组成的化合物的化学式是NH4Cl,该化合物属于离子化合物(填“离子”或“共价”);
(6)E、F两种元素的最高价氧化物的水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.