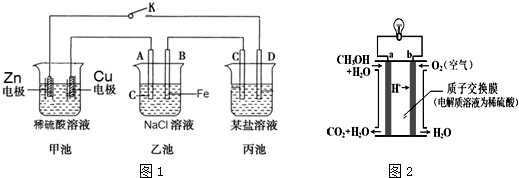
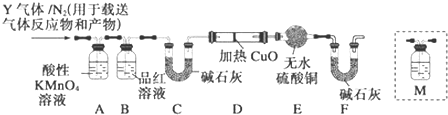
15.下列说法不正确的是( )
| A. | 0.02 mol•L-1醋酸与0.02 mol•L-1NaOH等体积混合后的溶液中加少量的CH3COONa固体则$\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$增大 | |
| B. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |
| C. | lmol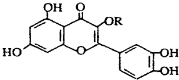 与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol 与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol | |
| D. | 红外光谱分析不能区分乙醇和乙醚 |
14.工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ•mol-1;
已知:N-N键能193kJ•mol-1,N≡N键能946kJ•mol-1
(1)按照轨道重叠方式可知,N2分子中共价键类型为σ键、π键,其中较稳定的是π键.
(2)合成氨常用铁系催化剂,写出基态铁原子价电子排布图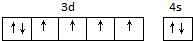 .
.
(3)在较高温度下,铁对氮气的强化学吸附是合成氨速率的决定步骤.其中一种吸附方式为: ,该吸附方式能加快反应速率的原因是氮氮三键变成了双键,结构发生改变.
,该吸附方式能加快反应速率的原因是氮氮三键变成了双键,结构发生改变.
(4)氨分子空间构型是三角锥,其氮原子采用的轨道杂化方式为sp3,氨是极性(填“极性”、“非极性”)分子,能与水分子形成氢键,易溶于水.固态氨是面心立方晶胞,有关数据如下表:
(5)固态氨晶体中氨分子的配位数12.
(6)列式计算固体氨的密度.
已知:N-N键能193kJ•mol-1,N≡N键能946kJ•mol-1
(1)按照轨道重叠方式可知,N2分子中共价键类型为σ键、π键,其中较稳定的是π键.
(2)合成氨常用铁系催化剂,写出基态铁原子价电子排布图
 .
.(3)在较高温度下,铁对氮气的强化学吸附是合成氨速率的决定步骤.其中一种吸附方式为:
 ,该吸附方式能加快反应速率的原因是氮氮三键变成了双键,结构发生改变.
,该吸附方式能加快反应速率的原因是氮氮三键变成了双键,结构发生改变.(4)氨分子空间构型是三角锥,其氮原子采用的轨道杂化方式为sp3,氨是极性(填“极性”、“非极性”)分子,能与水分子形成氢键,易溶于水.固态氨是面心立方晶胞,有关数据如下表:
| X射线衍射 | N-H键长 | N-N距离 | H-N-H键角 |
| 数据 | 101.9pm | 339.0pm | 107° |
(6)列式计算固体氨的密度.
13.在氨水与NH4HCO3混合溶液中滴入FeCl2溶液,不可能发生反应的离子方程式是( )
| A. | Fe2++2NH3•H2O═Fe(OH)2↓+2NH4+ | |
| B. | Fe2++NH3•H2O+HCO3-═FeCO3↓+NH4++H20 | |
| C. | Fe2++2HCO3-═Fe(OH)2↓+2CO2↑ | |
| D. | 2Fe2++HCO3-+3NH3•H2O═Fe2(OH)2CO3↓+3NH4++H2O |
12. 已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19.用0.1mol•L-1 NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19.用0.1mol•L-1 NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
0 155423 155431 155437 155441 155447 155449 155453 155459 155461 155467 155473 155477 155479 155483 155489 155491 155497 155501 155503 155507 155509 155513 155515 155517 155518 155519 155521 155522 155523 155525 155527 155531 155533 155537 155539 155543 155549 155551 155557 155561 155563 155567 155573 155579 155581 155587 155591 155593 155599 155603 155609 155617 203614
 已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19.用0.1mol•L-1 NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19.用0.1mol•L-1 NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )| A. | a点所得溶液中;2n(H2A)+n(A2-)=0.002mol | |
| B. | b点所得溶液中:c(H2A)+c(H+)=c(A2-)+e(OH-) | |
| C. | C点所得溶液中:c(Na+)<3c(HA-) | |
| D. | d点所得溶液中:c(Na+)>c(A2-)>c(HA-) |

 N2
N2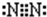 Na2O2
Na2O2 Mg3N2
Mg3N2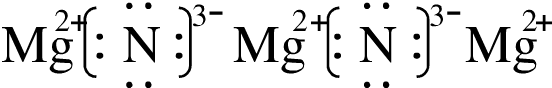
 .
.