1.(1)石灰工业对工农业生产意义重大,在制石灰的重要工业反应中包含着下列化学平衡:CaCO3(s)?CaO(s)+CO2(g)△H=+178.32kJ/mol现在800℃时,将CO2(g)、CaCO3(s)和CaO(s)按下列A~E不同的投料方式,放入一个10L的密闭容器中,经过足够长时间且维持温度不变,容器中CaCO3(s)的质量增加的有
A、减少的有C、D、E;体系处于化学平衡状态的有B(均填序号).(已知800℃时,该反应平衡常数K=0.003.)
(2)在岩洞、钟乳石的形成过程中包含下列反应:
CaCO3(s)+H2O(l)+CO2(g)?Ca2+(aq)+2HCO3-(aq)△H=-321.7kJ/mol
用一个不含c (Ca2+)、c (HCO3-)的表达式表示Ca (HCO3)2 溶液中的c (OH-)与其它粒子浓度间的关系:c (OH-)=c(H+)+c(H2CO3)-c(CO32-).
(3)为除去锅炉水垢中含有的CaSO4,可先用某溶液处理,使之转化为疏松、易溶于酸的物质,该转化的离子方程式是CaSO4(s)+CO32- (aq)?CaCO3(s )+SO42- (aq).
A、减少的有C、D、E;体系处于化学平衡状态的有B(均填序号).(已知800℃时,该反应平衡常数K=0.003.)
| 序号 | CaCO3/mol | CaO/mol | CO2/mol |
| A | 0.02 | 0.02 | 0.05 |
| B | 0.02 | 0.02 | 0.03 |
| C | 0.02 | 0.02 | 0.01 |
| D | 0.02 | 0 | 0.05 |
| E | 0.02 | 0.02 | 0 |
CaCO3(s)+H2O(l)+CO2(g)?Ca2+(aq)+2HCO3-(aq)△H=-321.7kJ/mol
用一个不含c (Ca2+)、c (HCO3-)的表达式表示Ca (HCO3)2 溶液中的c (OH-)与其它粒子浓度间的关系:c (OH-)=c(H+)+c(H2CO3)-c(CO32-).
(3)为除去锅炉水垢中含有的CaSO4,可先用某溶液处理,使之转化为疏松、易溶于酸的物质,该转化的离子方程式是CaSO4(s)+CO32- (aq)?CaCO3(s )+SO42- (aq).
17.氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
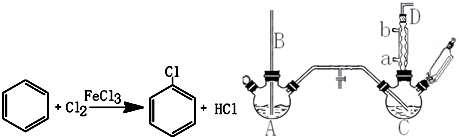
已知:氯苯为无色液体,沸点132.2℃.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是平衡气压.冷凝管中冷水应从a(填“a”或“b”) 处通入.
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是c(填序号)
酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、苯蒸气和氯气.
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;HCl+NaOH=NaCl+H2O(写两个即可).
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是五氧化二磷或氯化钙.
(5)工业生产中苯的流失情况如下:
则1t苯可制得成品为$\frac{(1-0.0892)×112.5}{78}$t(只要求列式).
0 155422 155430 155436 155440 155446 155448 155452 155458 155460 155466 155472 155476 155478 155482 155488 155490 155496 155500 155502 155506 155508 155512 155514 155516 155517 155518 155520 155521 155522 155524 155526 155530 155532 155536 155538 155542 155548 155550 155556 155560 155562 155566 155572 155578 155580 155586 155590 155592 155598 155602 155608 155616 203614

已知:氯苯为无色液体,沸点132.2℃.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是平衡气压.冷凝管中冷水应从a(填“a”或“b”) 处通入.
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是c(填序号)
酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、苯蒸气和氯气.
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;HCl+NaOH=NaCl+H2O(写两个即可).
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是五氧化二磷或氯化钙.
(5)工业生产中苯的流失情况如下:
| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |

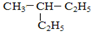 和
和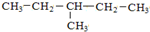
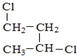 与
与 ④H2O和D2O
④H2O和D2O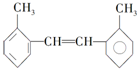 其苯环上的一氯代物有4种;1mol该物质和溴水混合,消耗Br2的物质的量为1mol.
其苯环上的一氯代物有4种;1mol该物质和溴水混合,消耗Br2的物质的量为1mol.


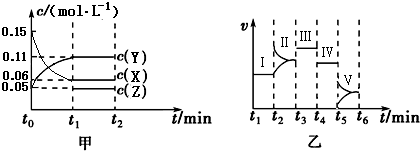
 2Y(g)+Z(g)△H=-10akJ/mol.在乙图Ⅰ~Ⅴ处平衡中,平衡常数最大的是Ⅴ.
2Y(g)+Z(g)△H=-10akJ/mol.在乙图Ⅰ~Ⅴ处平衡中,平衡常数最大的是Ⅴ.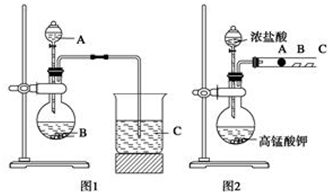
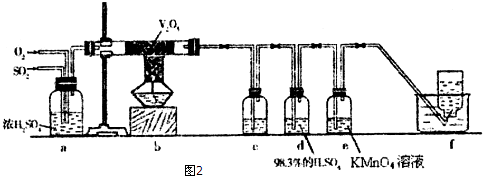
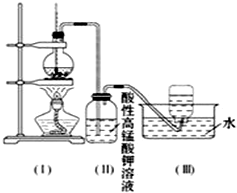 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后溶液中有黑色现象出现.过一段时间后,经硫酸酸化的高锰酸钾溶液褪色.经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O.
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后溶液中有黑色现象出现.过一段时间后,经硫酸酸化的高锰酸钾溶液褪色.经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O.