18.表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,X与Y的原子序数之和为Z与W原子序数之和的$\frac{2}{3}$.下列说法正确的是( )
| X | |||
| Y | Z | W | |
| T |
| A. | 化合物YX2、ZX2化学键类型和晶体类型均相同 | |
| B. | Z、W、T三种元素最高价氧化物的水化物的酸性依次增强 | |
| C. | 五种元素中,只有T是金属元素 | |
| D. | Mg在一定条件下可以和YX2发生反应生成Y单质 |
17.下列说法不正确的是( )
| A. | 危化品储存运输过程中发生金属钠、镁着火时,应立即用泡沫灭火器灭火 | |
| B. | 配制银氨溶液的操作:在2 mL 2%的硝酸银溶液中逐滴加入2%的氨水、振荡试管,直至产生的沉淀恰好完全溶解 | |
| C. | 配制230mL 0.1mol•L-1的FeCl3溶液:称取一定质量的FeCl3固体在烧杯中溶于适量盐酸中,放置至室温后,再转移入250mL容量瓶中进行配制 | |
| D. | 取少量硫酸亚铁铵晶体用蒸馏水溶解,加入适量10%的NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝色的气体,说明晶体中含有NH4+ |
16.下列说法不正确的是( )
| A. | 植物的秸秆、枝叶、杂草和人畜粪便等生物质在沼气池中经发酵可生成沼气 | |
| B. | Al(OH)3、Fe(OH)3等胶体具有很强的吸附能力,可用于净水 | |
| C. | 鸡蛋清中加入浓食盐水析出沉淀、75%乙醇溶液进行消毒、福尔马林用于浸制生物标本,其中蛋白质都发生了变性 | |
| D. | 塑料袋、废纸、旧橡胶制品等属于有机物,可以回收利用 |
14.在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:
A(g)?2B(g)+C(g)+D(s)△H=+85.1kJ•mol-1
容器内气体总压强(P)与起始压强P0的比值随反应时间(t)数据见下表:
回答下列问题:
(1)下列操作能提高A转化率的是AD
A.升高温度 B.体系中通入A气体
C.通入稀有气体He,使体系压强增大到原来的5倍
D.若体系中的C为HCl,其它物质均难溶于水,滴入少许水
(2)该反应的平衡常数的表达式K=$\frac{{c}^{2}(B)×c(C)}{c(A)}$,前2小时C的反应速率是0.02 mol•L-1•h-1
(3)平衡时A的转化率为70%.
A(g)?2B(g)+C(g)+D(s)△H=+85.1kJ•mol-1
容器内气体总压强(P)与起始压强P0的比值随反应时间(t)数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| $\frac{P}{{P}_{0}}$ | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
(1)下列操作能提高A转化率的是AD
A.升高温度 B.体系中通入A气体
C.通入稀有气体He,使体系压强增大到原来的5倍
D.若体系中的C为HCl,其它物质均难溶于水,滴入少许水
(2)该反应的平衡常数的表达式K=$\frac{{c}^{2}(B)×c(C)}{c(A)}$,前2小时C的反应速率是0.02 mol•L-1•h-1
(3)平衡时A的转化率为70%.
13.高锰酸钾是中学化学常用的强氧化剂,实验室中可通过以下反应制得:
MnO2熔融氧化:3MnO2+KClO3+6KOH$\frac{\underline{\;熔化\;}}{\;}$3K2MnO4+KCl+3H2O
K2MnO4歧化:3K2MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度数据见下表:
实验流程如下:

已知K2MnO4溶液显绿色,KMnO4溶液紫红色.请回答下列问题:
(1)步骤①应在D中熔化,并用铁棒用力搅拌,以防结块.
A.烧杯 B.蒸发皿 C.瓷坩埚 D.铁坩埚
(2)综合相关物质的化学性质及溶解度,步骤③中可以替代CO2的试剂是B.
A.二氧化硫 B.醋酸 C.盐酸 D.硫酸
(3)下列监控K2MnO4歧化完全的方法或操作可行的是B.
A.通过观察溶液颜色变化,若溶液颜色由绿色完全变成紫红色,表明反应已歧化完全
B.取上层清液少许于试管中,继续通入CO2,若无沉淀产生,表明反应已歧化完全
C.pH试纸测定溶液的pH值,对照标准比色卡,若pH为10~11,表明反应已歧化完全
(4)当溶液pH值达10~11时,停止通CO2;若CO2过多,造成的后果是二氧化碳和碳酸钾反应生成碳酸氢钾,结晶时会同高锰酸钾一起析出,产品纯度降低.
(5)烘干时,温度控制在80℃为宜,温度不宜过高的理由是如果温度过低,烘干时间过长,如果温度过高,高锰酸钾受热分解.
(6)通过用草酸滴定酸化后的KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数).
①滴定过程溶液中发生的离子反应为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
②称量w g KMnO4粗产品配制成100ml待测溶液,配制过程中除玻璃棒和烧杯外还需要用到的玻璃仪器有100ml容量瓶、胶头滴管.
③量取KMnO4待测液10.00ml,若该滴定管用蒸馏水洗净后未润洗,则测定结果将偏小.
④滴定终点溶液的颜色变化是溶液由红色变无色.
⑤经测定每滴定10.00ml待测液平均消耗c mol/L草酸标准液Vml,样品纯度的表达式为$\frac{CVM}{250W}$×100%(高锰酸钾摩尔质量用M表示).
MnO2熔融氧化:3MnO2+KClO3+6KOH$\frac{\underline{\;熔化\;}}{\;}$3K2MnO4+KCl+3H2O
K2MnO4歧化:3K2MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度数据见下表:
| 20℃ | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| s(g/100g水) | 111 | 33.7 | 11.1 | 6.34 |

已知K2MnO4溶液显绿色,KMnO4溶液紫红色.请回答下列问题:
(1)步骤①应在D中熔化,并用铁棒用力搅拌,以防结块.
A.烧杯 B.蒸发皿 C.瓷坩埚 D.铁坩埚
(2)综合相关物质的化学性质及溶解度,步骤③中可以替代CO2的试剂是B.
A.二氧化硫 B.醋酸 C.盐酸 D.硫酸
(3)下列监控K2MnO4歧化完全的方法或操作可行的是B.
A.通过观察溶液颜色变化,若溶液颜色由绿色完全变成紫红色,表明反应已歧化完全
B.取上层清液少许于试管中,继续通入CO2,若无沉淀产生,表明反应已歧化完全
C.pH试纸测定溶液的pH值,对照标准比色卡,若pH为10~11,表明反应已歧化完全
(4)当溶液pH值达10~11时,停止通CO2;若CO2过多,造成的后果是二氧化碳和碳酸钾反应生成碳酸氢钾,结晶时会同高锰酸钾一起析出,产品纯度降低.
(5)烘干时,温度控制在80℃为宜,温度不宜过高的理由是如果温度过低,烘干时间过长,如果温度过高,高锰酸钾受热分解.
(6)通过用草酸滴定酸化后的KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数).
①滴定过程溶液中发生的离子反应为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
②称量w g KMnO4粗产品配制成100ml待测溶液,配制过程中除玻璃棒和烧杯外还需要用到的玻璃仪器有100ml容量瓶、胶头滴管.
③量取KMnO4待测液10.00ml,若该滴定管用蒸馏水洗净后未润洗,则测定结果将偏小.
④滴定终点溶液的颜色变化是溶液由红色变无色.
⑤经测定每滴定10.00ml待测液平均消耗c mol/L草酸标准液Vml,样品纯度的表达式为$\frac{CVM}{250W}$×100%(高锰酸钾摩尔质量用M表示).
10.利用化石燃料开采、加工过程产生的H2S废气,通过电化学法制取氢气的工艺如图,下列说法不正确的是( )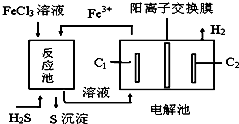

| A. | 电解池中惰性电极C1为阳极 | |
| B. | 该工艺优点之一是FeCl3溶液可循环利用 | |
| C. | 反应池中的离子方程式:2Fe3++S2-=2Fe2++S↓ | |
| D. | 电解池总反应的化学方程式:2FeCl2+2HCl$\frac{\underline{\;通电\;}}{\;}$2FeCl3+H2↑ |
9.下列各示意图与对应表述正确的是( )
0 155416 155424 155430 155434 155440 155442 155446 155452 155454 155460 155466 155470 155472 155476 155482 155484 155490 155494 155496 155500 155502 155506 155508 155510 155511 155512 155514 155515 155516 155518 155520 155524 155526 155530 155532 155536 155542 155544 155550 155554 155556 155560 155566 155572 155574 155580 155584 155586 155592 155596 155602 155610 203614
| A. |  为证明非金属性强弱:S>C>Si | |
| B. | 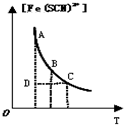 表示可逆反应Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)平衡时,物质的量浓度[Fe(SCN)2+]与温度T的关系,反应处于D点时,一定有V(正)<V(逆) | |
| C. | 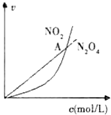 表示恒温恒容条件下发生的可逆反应2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| D. | 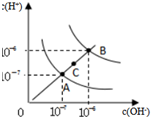 为水的电离平衡曲线图,若从A点到C点,可在水中加入适量NaOH固体 |
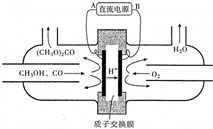 (1)在425℃、A12O3作催化剂,甲醇与氨气反应可以制得二甲胺(CH3)2NH.二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-).
(1)在425℃、A12O3作催化剂,甲醇与氨气反应可以制得二甲胺(CH3)2NH.二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-).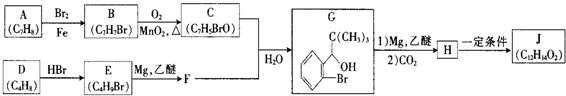
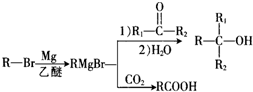
 .
. +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$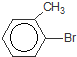 +HBr,反应类型为取代反应.
+HBr,反应类型为取代反应.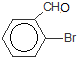 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. .
. 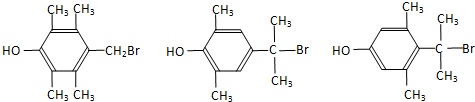 任意2种.
任意2种.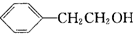
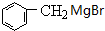 .
.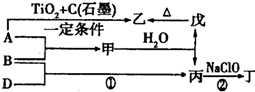
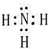 ,丁中所包含的化学键类型有bc(填字母序号).
,丁中所包含的化学键类型有bc(填字母序号).