16.根据下表中五种元素的电离能数据(单位:kJ•mol-1),下列说法不正确的是( )
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| u | 420 | 3100 | 4400 | 5900 |
| A. | T的氯化物最可能的化学式为TCl3 | |
| B. | 氦元素最有可能与Q元素位于同一族 | |
| C. | 在同周期表中,最可能处于同一族的是R和U | |
| D. | U元素最有可能为K,R元素最有可能为Li |
15.晶体是一类非常重要的材料,在很多领域都有广泛的应用.我国现已能够拉制出直径为300毫米,重量达81千克的大直径硅单晶,晶体硅大量用于电子产业.下列对晶体硅的叙述正确的是( )
| A. | 晶体硅没有固定的熔沸点 | |
| B. | 形成晶体硅的速率越快越好 | |
| C. | 可用于X-射线衍射实验来鉴别晶体硅和玻璃 | |
| D. | 晶体硅的形成与晶体的自范性有关,形成的晶体无各向异性 |
14.不法商人将有毒的三聚氰胺(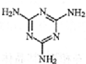 )添加于奶粉中,增加奶粉中的含氮量.下列关于三聚氰胺分子的说法正确的是( )
)添加于奶粉中,增加奶粉中的含氮量.下列关于三聚氰胺分子的说法正确的是( )
 )添加于奶粉中,增加奶粉中的含氮量.下列关于三聚氰胺分子的说法正确的是( )
)添加于奶粉中,增加奶粉中的含氮量.下列关于三聚氰胺分子的说法正确的是( )| A. | 形成的晶体熔点较高 | |
| B. | 一个分子中共含有15个σ键 | |
| C. | 属于极性分子,故极易溶于水 | |
| D. | 所有面原子采用sp2杂化,所有氮原子采用sp3杂化 |
13.下列排序错误的是( )
| A. | 熔点由高到低:NaCl>Na-K合金>Na | |
| B. | 晶体的熔点由低到高:CF4<CCl4<CBr4<CI4 | |
| C. | 晶体的硬度由大到小:金刚石>碳化硅>晶体硅 | |
| D. | 晶体的晶格能由大到小:NaF>NaCl>NaBr>NaI |
12.下列说法正确的是( )
| A. | 分子晶体在水中溶解时,只破坏分子间作用力 | |
| B. | 原子晶体中的各相邻原子都以非极性键相结合 | |
| C. | 分子晶体的熔沸点很低,常温下都呈液态或气态 | |
| D. | 含有金属阳离子的晶体不一定是离子晶体 |
11.下列关于杂化轨道的叙述中,不正确的是( )
| A. | 分子中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 | |
| B. | 杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 | |
| C. | 若AB2分子的构型为V型,则A可能为sp2杂化 | |
| D. | H2S和SO2分子中的中心原子杂化类型相同 |
10.下列有关σ键和π键的说法错误的是( )
| A. | σ键的特征是轴对称,π键的特征是镜面对称 | |
| B. | 气体单质中一定有σ键,可能有π键 | |
| C. | 乙烯与氢气发生加成反应时,乙烯分子中有π键断裂 | |
| D. | 当原子形成分子时,首先形成σ键,可能形成π键 |
9.在硼酸[B(OH)3 ]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构.则晶体中同层分子间的主要作用力是( )
0 155400 155408 155414 155418 155424 155426 155430 155436 155438 155444 155450 155454 155456 155460 155466 155468 155474 155478 155480 155484 155486 155490 155492 155494 155495 155496 155498 155499 155500 155502 155504 155508 155510 155514 155516 155520 155526 155528 155534 155538 155540 155544 155550 155556 155558 155564 155568 155570 155576 155580 155586 155594 203614
| A. | 范德华力 | B. | 共价键 | C. | 氢键 | D. | 离子键 |
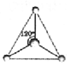 CH3+;
CH3+;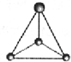 CH3-.
CH3-.