17.下表列出了某短周期元素R的各级电离能数据(用I1、I2…表示,单位为kJ•mol-1).下列关于元素R的判断中一定正确的是( )
①R的最高正价为+3价
②R元素位于元素周期表中第ⅡA族
③R元素第一电离能大于同周期相邻元素
④R元素的原子最外层共有4个电子
⑤R元素基态原子的电子排布式为1s22s2.
| I1 | I2 | I3 | I4 | I5 | … | |
| R | 740 | 1500 | 7700 | 10500 | 13600 | … |
②R元素位于元素周期表中第ⅡA族
③R元素第一电离能大于同周期相邻元素
④R元素的原子最外层共有4个电子
⑤R元素基态原子的电子排布式为1s22s2.
| A. | ①③ | B. | ②③ | C. | ②③④ | D. | ②③⑤ |
16.下列说法正确的是( )
| A. | 电子云伸展方向与电子的能量大小是无关的 | |
| B. | 只含极性键的分子一定是极性分子 | |
| C. | 氢键是一种特殊的化学键,它广泛地存在于自然界中 | |
| D. | H-O键键能为462.8 kJ/mol,即18 g H2O分解成H2和O2时,消耗能量为2×462.8 kJ |
15.在10L恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g)?2C(g)+D(s),所得实验数据如下表,下列说法正确的是( )
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(A) | n(B) | n(C) | ||
| ① | 700 | 4.0 | 1.0 | 1.80 |
| ② | 800 | 1.0 | 4.0 | 1.60 |
| ③ | 800 | 2.0 | 2.0 | a |
| ④ | 900 | 1.0 | 1.0 | b |
| A. | 实验①中,若10min达到平衡,则v(D)=9.0×10-2mol/(L•min) | |
| B. | 实验②中,该反应的平衡常数K=3.2 | |
| C. | 实验③中,达到平衡时A的转化率为60% | |
| D. | 实验④中,达到平衡时,b<1.0 |
13.某元素原子核外M层电子数是L层电子数的一半,则此元素是( )
| A. | Li | B. | C | C. | Si | D. | S |
12.实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
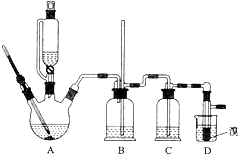
有关数据列表如下:
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收A中反应可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收A中反应可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
11.某烃含碳、氢原子物质的量之比为1:2,该烃对氮气的相对密度为2,该烃可使溴水褪色,该烃的二氯代物有四种同分异构体,该烃为( )
| A. | CH3CH2CH2CH3 | B. | CH2=CH-CH3 | C. | CH2=CH-CH2-CH3 | D. | CH2=C(CH3)2 |
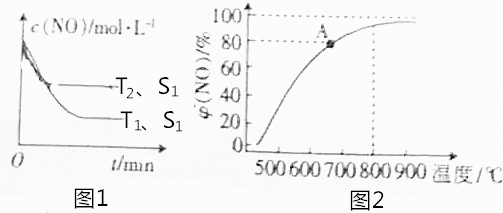
10.(1)HNO3与金属反应情况多种多样.为探究HNO3性质,某兴趣小组作如下探究:用浓硝酸和水按照不同体积比配成不同浓度的硝酸溶液,各取10mL硝酸溶液分别与铜片反应,实验记录如下:
制备NO气体最适宜的是:实验Ⅱ,理由是:产物是NO,反应速率较快(不用加热).
(2)兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠.设计装置如下(忽略装置中空气的影响),请回答下列问题:

①组装好仪器后,必须进行的一项操作是:检查装置的气密性.
②推测B中可以观察到的主要现象是:铜片逐渐溶解,溶液逐渐变蓝,产生无色气泡;C装置的作用是:除去NO中混有的CO2.
③装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是:NaOH.可以通过适当改进,不产生Y物质,请你提出改进方法:用装有碱石灰的干燥管代替C装置.
④E装置的实验目的是:尾气处理,防止有害气体对大气污染.
0 155398 155406 155412 155416 155422 155424 155428 155434 155436 155442 155448 155452 155454 155458 155464 155466 155472 155476 155478 155482 155484 155488 155490 155492 155493 155494 155496 155497 155498 155500 155502 155506 155508 155512 155514 155518 155524 155526 155532 155536 155538 155542 155548 155554 155556 155562 155566 155568 155574 155578 155584 155592 203614
| 序号 | 浓硝酸与水的体积比 | 实 验 现 象 |
| Ⅰ | 1﹕1 | 反应速率快,溶液很快变成蓝色,铜丝表面有大量气泡冒出,气体呈红棕色 |
| Ⅱ | 1﹕3 | 反应速率较快,溶液变成蓝色,铜丝表面有大量气泡冒出,气体无色 |
| Ⅲ | 1﹕5 | 反应速率慢,微热后速率加快,溶液变成蓝色,铜丝表面有气泡冒出,气体无色 |
(2)兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠.设计装置如下(忽略装置中空气的影响),请回答下列问题:

①组装好仪器后,必须进行的一项操作是:检查装置的气密性.
②推测B中可以观察到的主要现象是:铜片逐渐溶解,溶液逐渐变蓝,产生无色气泡;C装置的作用是:除去NO中混有的CO2.
③装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是:NaOH.可以通过适当改进,不产生Y物质,请你提出改进方法:用装有碱石灰的干燥管代替C装置.
④E装置的实验目的是:尾气处理,防止有害气体对大气污染.
 如图是实验室制取某些气体的装置.
如图是实验室制取某些气体的装置.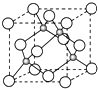 A、B、C是短周期非金属元素,核电荷数依次增大.A元素原子核外有三种不同的能级且各个能级所填充的电子数相同,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空:
A、B、C是短周期非金属元素,核电荷数依次增大.A元素原子核外有三种不同的能级且各个能级所填充的电子数相同,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空: