5.部分弱酸的电离常数如下表:
(1)同温同物质的量浓度的HCOONa(aq)与NaClO(aq)中pH大的是NaClO(aq).
(2)1molCl2与2molNa2CO3(aq)反应除生成NaCl外还有NaHCO3、NaClO(填化学式).
(3)向一定量的NaHCO3(aq)中通入少量的SO2(g),反应的离子方程式为HCO3-+SO2→HSO3-+CO2↑.
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性.
(4)将亚硒酸与高锰酸钾共热可制得硒酸(H2SeO4),配平该反应方程式,并标出电子转移
的方向和数目.
5H2SeO3+2KMnO4→1K2SeO4+2MnSeO4+2H2SeO4+3H2O
(5)与硫同族的元素Te,最高价氧化物的水化物碲酸(H6TeO6)的酸性比H2SO4弱(选填“强”或“弱”),其氧化性比硫酸强.向碲酸中通入SO2气体,若反应中生成的TeO2与Te的物质的量之比为2:1,写出该反应的化学方程式5SO2+3H6TeO6→2TeO2+Te+5H2SO4+4H2O.当6mol碲酸与一定量SO2恰好完全反应,所得溶液体积为20L,则所得溶液的pH为0.
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离常数 (25℃) | Ki=1.77×10-4 | Kii=2.98×10-6 | K1Ki1=4.3×10-7 Ki2=5.6×10-11 | Ki1=1.54×10-2 Ki2=5.6×10-7 |
(2)1molCl2与2molNa2CO3(aq)反应除生成NaCl外还有NaHCO3、NaClO(填化学式).
(3)向一定量的NaHCO3(aq)中通入少量的SO2(g),反应的离子方程式为HCO3-+SO2→HSO3-+CO2↑.
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性.
(4)将亚硒酸与高锰酸钾共热可制得硒酸(H2SeO4),配平该反应方程式,并标出电子转移
的方向和数目.
5H2SeO3+2KMnO4→1K2SeO4+2MnSeO4+2H2SeO4+3H2O
(5)与硫同族的元素Te,最高价氧化物的水化物碲酸(H6TeO6)的酸性比H2SO4弱(选填“强”或“弱”),其氧化性比硫酸强.向碲酸中通入SO2气体,若反应中生成的TeO2与Te的物质的量之比为2:1,写出该反应的化学方程式5SO2+3H6TeO6→2TeO2+Te+5H2SO4+4H2O.当6mol碲酸与一定量SO2恰好完全反应,所得溶液体积为20L,则所得溶液的pH为0.
3.甲、乙两种CH3COOH溶液的pH,若甲比乙大1,则甲、乙两溶液中( )
0 155391 155399 155405 155409 155415 155417 155421 155427 155429 155435 155441 155445 155447 155451 155457 155459 155465 155469 155471 155475 155477 155481 155483 155485 155486 155487 155489 155490 155491 155493 155495 155499 155501 155505 155507 155511 155517 155519 155525 155529 155531 155535 155541 155547 155549 155555 155559 155561 155567 155571 155577 155585 203614
| A. | c(甲):c(乙)=1:10 | B. | c(H+)甲:c(H+)乙=1:2 | ||
| C. | c(OH-)甲:c(OH-)乙=10:1 | D. | a(甲):a(乙)=2:1 |
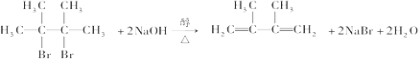 ;
;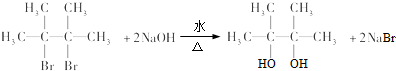 ;E与乙二醇的关系是同系物.
;E与乙二醇的关系是同系物. .
.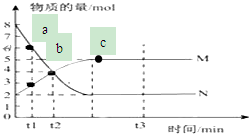 一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示: ]2-,CO2的结构式为O=C=O.与镁同周期、离子半径最小的元素,其原子最外层的电子排布式为3s23p1,其中能量最高的电子有1个.
]2-,CO2的结构式为O=C=O.与镁同周期、离子半径最小的元素,其原子最外层的电子排布式为3s23p1,其中能量最高的电子有1个.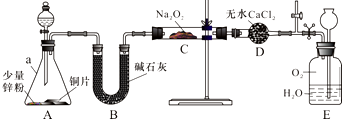 NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究.
NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究.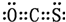 ;碳原子核外电子的轨道表达式为
;碳原子核外电子的轨道表达式为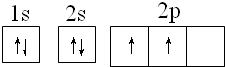 .
.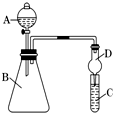 Ⅰ.某同学为探究元素周期表中同周期元素性质的递变规律,设计了如下系列实验.
Ⅰ.某同学为探究元素周期表中同周期元素性质的递变规律,设计了如下系列实验.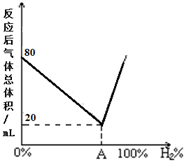 ①某烷烃分子式为C6H14,若该烷烃可由两种炔烃与氢气加成得到,则该烷烃的结构简式为(CH3)2CHCH2CH2CH3.
①某烷烃分子式为C6H14,若该烷烃可由两种炔烃与氢气加成得到,则该烷烃的结构简式为(CH3)2CHCH2CH2CH3.