20.如图所示,将纯Fe棒和石墨棒插入1L饱和NaCl溶液中.下列说法正确的是( )
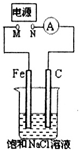

| A. | M连接电源正极,N连接电源负极,当两极产生气体总量为22.4mL(标准状况)时,则生成0.001molNaOH | |
| B. | 去掉电源,将M、N用导线直接相连,在溶液中滴入酚酞试液,C电极周围溶液变红 | |
| C. | M连接电源负极,N连接电源正极,如果把烧杯中的溶液换成1LCuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 | |
| D. | M连接电源正极,N连接电源负极,将C电极换成Cu电极,电解质溶液换成硫酸铜溶液,则可实现在铁上镀铜 |
19.钠离子电池具有资源广泛、价格低廉、环境友好、安全可靠的特点,特别适合于固定式大规模储能应用的需求.一种以Na2SO4水溶液为电解液的钠离子电池总反应为:
NaTi2(PO4)3+2Na2NiFeⅡ(CN)6 $?_{充电}^{放电}$ Na3Ti2(PO4)3+2NaNiFeⅢ(CN)6
(注:其中P的化合价为+5,Fe的上标Ⅱ、Ⅲ代表其价态).下列说法不正确的是( )
NaTi2(PO4)3+2Na2NiFeⅡ(CN)6 $?_{充电}^{放电}$ Na3Ti2(PO4)3+2NaNiFeⅢ(CN)6
(注:其中P的化合价为+5,Fe的上标Ⅱ、Ⅲ代表其价态).下列说法不正确的是( )
| A. | 放电时NaTi2(PO4)3在正极发生还原反应 | |
| B. | 放电时负极材料中的Na+脱离电极进入溶液,同时溶液中的Na+嵌入到正极材料中 | |
| C. | 充电过程中阳极反应式为:2NaNiFeIIⅢ(CN)6+2Na++2e-=2Na2NiFeⅡ(CN)6 | |
| D. | 该电池在较长时间的使用过程中电解质溶液中Na+的浓度基本保持不变 |
18.下列有关钢铁腐蚀与防护的说法正确的是( )
| A. | 钢管与铅连接,钢管可被保护 | |
| B. | 铁遇冷浓硫酸表面钝化,可保护内部不被腐蚀 | |
| C. | 纯铁比生铁更容易被腐蚀 | |
| D. | 钢铁发生析氢腐蚀时,负极反应是Fe-3e-═Fe3+ |
17.如图是碳的正常循环,但由于过度燃烧化石燃料,造成二氧化碳浓度不断上升.研究和解决二氧化碳捕集、存储和转化问题成为当前化学工作者的重要使命.
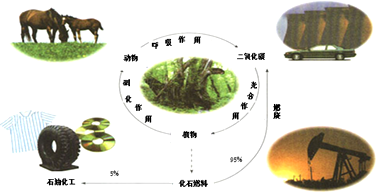
(1)有关碳循环的说法中正确的是ac
a.光合作用是光能转化成化学能b.化石燃料是可再生的
c.循环过程有氧化还原反应d.石油中含乙烯、丙烯,通过加聚反应得到高分子化合物
(2)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2发生反应:2CO2(g)=2CO(g)+O2(g),该反应的△H0>,(选填:>、<、=).
(3)CO2转化途径之一是:利用太阳能或生物质能分解水制H2,然后将H2与CO2转化为甲醇或其它的物质.
2H2O(1)=2H2(g)+O2(g)△H=+571.5kJ•mol-1
3H2(g)+CO2(g)=CH3OH(l)+H2O(1)△H=-137.8kJ•mol-1
则反应:4H2O (1)+2CO2(g)=2CH3OH(l)+3O2(g)△H=kJ•mol-1.
你认为该方法需要解决的技术问题有:.
a.开发高效光催化剂
b.将光催化制取的氢气从反应体系中有效分离,并与CO2催化转化.
c.二氧化碳及水资源的来源供应
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见下表.( t1<t2<t3)
氨基甲酸铵分解反应是吸热反应(“放热”、“吸热”).在15℃,此反应的化学平衡常数为:4×10-6.
(5)用一种钾盐水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图).在阴极上产生乙烯的电极反应方程式为:2CO2+12H++12e-=CH2=CH2+4H2O.


(1)有关碳循环的说法中正确的是ac
a.光合作用是光能转化成化学能b.化石燃料是可再生的
c.循环过程有氧化还原反应d.石油中含乙烯、丙烯,通过加聚反应得到高分子化合物
(2)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2发生反应:2CO2(g)=2CO(g)+O2(g),该反应的△H0>,(选填:>、<、=).
(3)CO2转化途径之一是:利用太阳能或生物质能分解水制H2,然后将H2与CO2转化为甲醇或其它的物质.
2H2O(1)=2H2(g)+O2(g)△H=+571.5kJ•mol-1
3H2(g)+CO2(g)=CH3OH(l)+H2O(1)△H=-137.8kJ•mol-1
则反应:4H2O (1)+2CO2(g)=2CH3OH(l)+3O2(g)△H=kJ•mol-1.
你认为该方法需要解决的技术问题有:.
a.开发高效光催化剂
b.将光催化制取的氢气从反应体系中有效分离,并与CO2催化转化.
c.二氧化碳及水资源的来源供应
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见下表.( t1<t2<t3)
| 温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
(5)用一种钾盐水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图).在阴极上产生乙烯的电极反应方程式为:2CO2+12H++12e-=CH2=CH2+4H2O.

15.下列过程不涉及氧化还原反应的是( )
| A. |  火法炼铜 | B. |  中和滴定 | C. |  酿酒 | D. |  制眼镜 |
12.向10mL0.10mol•L-1某一元酸HA溶液中滴加等浓度的NaOH溶液,滴加过程溶液的pH随滴加NaOH溶液体积的变化如图所示,下列叙述正确的是( )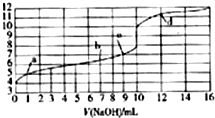

| A. | HA为一元强酸 | |
| B. | 水的电离程度:a点>b点>c点 | |
| C. | c点时,酸和碱恰好完全反应 | |
| D. | d点时,溶液中离子浓度:c(Na+)>c(A-)>c(OH-)>c(H+) |
11. 图甲是在微生物的作用下将有机废水(主要含有葡萄糖)的化学能转化为电能的装置,图乙是用情性电极电解饱和食盐水制取一种家用消毒液的装置,下列说法错误的是( )
图甲是在微生物的作用下将有机废水(主要含有葡萄糖)的化学能转化为电能的装置,图乙是用情性电极电解饱和食盐水制取一种家用消毒液的装置,下列说法错误的是( )
0 155383 155391 155397 155401 155407 155409 155413 155419 155421 155427 155433 155437 155439 155443 155449 155451 155457 155461 155463 155467 155469 155473 155475 155477 155478 155479 155481 155482 155483 155485 155487 155491 155493 155497 155499 155503 155509 155511 155517 155521 155523 155527 155533 155539 155541 155547 155551 155553 155559 155563 155569 155577 203614
 图甲是在微生物的作用下将有机废水(主要含有葡萄糖)的化学能转化为电能的装置,图乙是用情性电极电解饱和食盐水制取一种家用消毒液的装置,下列说法错误的是( )
图甲是在微生物的作用下将有机废水(主要含有葡萄糖)的化学能转化为电能的装置,图乙是用情性电极电解饱和食盐水制取一种家用消毒液的装置,下列说法错误的是( )| A. | M电极的电极反应式为:C6H12O6-24e-+6H2O═6CO2↑+24H+ | |
| B. | N电极上每消耗22.4L气体(标准状况)时,则有4molH+通过质子交换膜从负极区移向正极区 | |
| C. | 若装置乙所需的电能来自装置甲,则b极应与X极连接 | |
| D. | 由装置乙制得的家用消毒液的有效成分是NaClO |
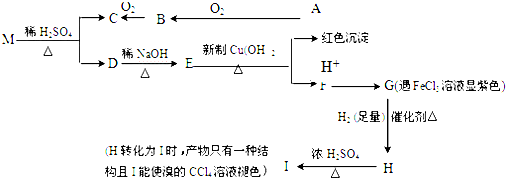
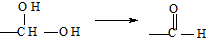
 ;②H→I:
;②H→I: .
. .
.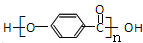 .
. 等.(任写一种)
等.(任写一种)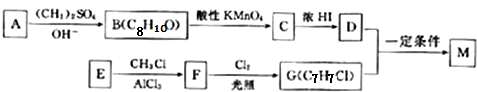
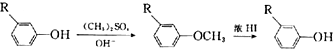
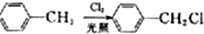
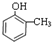 ;E→F的反应类型为取代反应.
;E→F的反应类型为取代反应.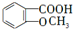 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$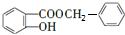 +HCl
+HCl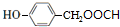 (写结构简式).
(写结构简式). 和(CH2)3CCl为起始原料制备
和(CH2)3CCl为起始原料制备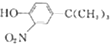 的合成路线:
的合成路线: $→_{AlCl_{3}}^{(CH_{3})_{3}CCl}$
$→_{AlCl_{3}}^{(CH_{3})_{3}CCl}$ $→_{OH-}^{(CH_{3})_{2}SO_{4}}$
$→_{OH-}^{(CH_{3})_{2}SO_{4}}$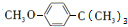 $→_{浓H_{2}O_{4}/△}^{浓HNO_{3}}$
$→_{浓H_{2}O_{4}/△}^{浓HNO_{3}}$ $\stackrel{浓HI}{→}$
$\stackrel{浓HI}{→}$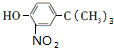 .
.
