20.下列实验能达到实验目的且符合安全要求的是( )
| A. | 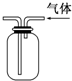 利用排空气法收集CO2 | B. |  收集氧气 | ||
| C. | 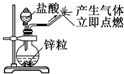 制备并检验氢气的可燃性 | D. | 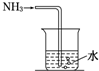 氨水溶于水 |
17.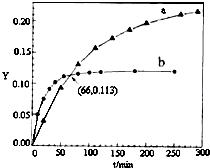 已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )
已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )
 已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )
已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )| A. | b代表20℃下CH3COCH3的Y-t曲线 | |
| B. | 从Y=0到Y=0.113,CH3COCH2COH(CH3)2的$\frac{△n(0℃)}{△n(20℃)}$=1 | |
| C. | 升高温度可缩短反应达平衡的时间并能提高平衡转化率 | |
| D. | 反应进行到20min末,CH3COCH3的$\frac{v(0℃)}{v(20℃)}$<1 |
16.取浓度相同的NaOH和HCl溶液,以2:3体积比相混合,所得溶液的pH等于1,则原溶液的浓度为( )
| A. | 0.01 mol•L-1 | B. | 0.017 mol•L-1 | C. | 0.05 mol•L-1 | D. | 0.50 mol•L-1 |
15.已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-25kJ•mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47kJ•mol-1
则下列关于Fe3O4(s)被CO还原成Fe(s)和CO2的热化学方程式的书写中正确的是( )
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-25kJ•mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47kJ•mol-1
则下列关于Fe3O4(s)被CO还原成Fe(s)和CO2的热化学方程式的书写中正确的是( )
| A. | Fe3O4+4CO=3Fe+4CO2△H=-14kJ•mol-1 | |
| B. | Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)△H=-22kJ•mol-1 | |
| C. | Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)△H=+14kJ•mol-1 | |
| D. | Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)△H=-14kJ•mol-1 |
14.下列实验对应的结论不正确的是( )
| A. | 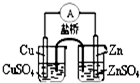 能组成Zn、Cu原电池 | B. |  能证明非金属性C>Si | ||
| C. | 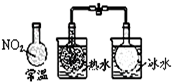 说明反应2NO2?N2O4△H>0 | D. | 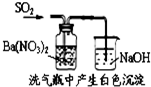 白色沉淀为BaSO4 |
13.下列说法正确的是( )
| A. | 常温下,由水电离出的c(H+)=10-12mol/L,则溶液pH一定为12 | |
| B. | 已知H2C2O4是弱酸,其电离方程式为:H2C2O4?2H++C2O42- | |
| C. | 常温下,pH=10的氨水溶液中,由水电离出的c(H+)=10-10mol/L | |
| D. | 工业合成氨温度控制在500℃,目的是为了提高产率 |
11.下列关于热化学的说法正确的是( )
0 155347 155355 155361 155365 155371 155373 155377 155383 155385 155391 155397 155401 155403 155407 155413 155415 155421 155425 155427 155431 155433 155437 155439 155441 155442 155443 155445 155446 155447 155449 155451 155455 155457 155461 155463 155467 155473 155475 155481 155485 155487 155491 155497 155503 155505 155511 155515 155517 155523 155527 155533 155541 203614
| A. | 需要加热才能发生的反应是吸热反应 | |
| B. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出热量少 | |
| C. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 | |
| D. | 由热化学方程式 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
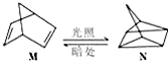 △H=+88.6kJ/mol
△H=+88.6kJ/mol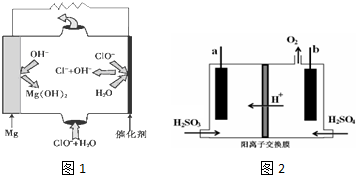
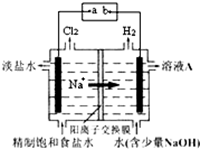 氯碱工业中电解饱和食盐水的原理示意图如图所示.
氯碱工业中电解饱和食盐水的原理示意图如图所示.