6. W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第VIA族;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是Cl->N3->O2->Na+(用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、Cl2、ClO2 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是H2S(填化学式),沸点高的是H2O(填化学式)
(6)ZW的电子式为Na+[:H]-,W2Y2的电子式为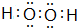 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: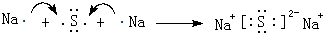 .
.
(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液不褪色(填“褪色”或“不褪色”),请用相关离子方程式解释原因SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
(8)已知
工业制镁时,电解MgCl2而不电解MgO的原因是氧化镁熔点高,耗能多;制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融时不导电.
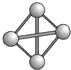
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N入出942kJ.根据以上信息和数据,下列说法正确的是C.
A.N4属于一种新型化合物
B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2
D.1molN4转变为N2将吸收882KJ的能量.
 W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第VIA族;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是Cl->N3->O2->Na+(用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、Cl2、ClO2 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是H2S(填化学式),沸点高的是H2O(填化学式)
(6)ZW的电子式为Na+[:H]-,W2Y2的电子式为
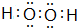 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: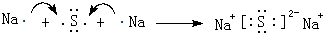 .
.(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液不褪色(填“褪色”或“不褪色”),请用相关离子方程式解释原因SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
(8)已知
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N入出942kJ.根据以上信息和数据,下列说法正确的是C.
A.N4属于一种新型化合物
B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2
D.1molN4转变为N2将吸收882KJ的能量.
5.下列有关元素的性质及其递变规律正确的是( )
| A. | IA族与ⅦA族元素间形成的化合物都是离子化合物 | |
| B. | 第三周期元素从左到右,最高正价从+1递增到+7 | |
| C. | 同主族元素的简单阴离子从上到下还原性减弱 | |
| D. | 同周期金属元素的化合价越高,其原子失电子能力越强 |
4.某饱和一氯代烷3.70g与足量的NaOH水溶液混合加热后,用HNO3酸化,再加入足量AgNO3溶液,生成白色沉淀5.74g.则该卤代烃的分子式为:C4H9Cl,这种一氯代物的同分异构体种类有4种.
3.下列叙述正确的是( )


| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 在一定条件下,化合物Y可与Br2发生加成反应 | |
| C. | 用FeCl3溶液可鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
2.分子式为C10H14的一取代芳香烃,其可能的结构有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
1.(1)由A、B、C、D四种金属按表中装置进行实验.
根据实验现象回答下列问题:
①装置甲中负极的电极反应为A-2e-═A2+.
②装置乙中正极的电极反应为Cu2++2e-═Cu.
③装置丙中溶液的pH增大(填“增大”、“减小”或“不变”).
④四种金属活动性由强到弱的顺序为D>A>B>C.
(2)在一定温度下,反应2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)达到平衡状态时,n(SO2):n(O2):n (SO3)=2:3:4.缩小体积,再次达到平衡状态时,n(O2)=0.8mol,n(SO3)=1.4mol,下列说法正确的是AB.
A.再次达到平衡状态时,n(SO2)为0.4mol B.缩小体积,再次达到平衡过程中,v正>v逆
C.使用催化剂对反应速率影响不大 D.工业上一般采用增加SO2的浓度来提高O2的转化率.
0 155346 155354 155360 155364 155370 155372 155376 155382 155384 155390 155396 155400 155402 155406 155412 155414 155420 155424 155426 155430 155432 155436 155438 155440 155441 155442 155444 155445 155446 155448 155450 155454 155456 155460 155462 155466 155472 155474 155480 155484 155486 155490 155496 155502 155504 155510 155514 155516 155522 155526 155532 155540 203614
| 实验装置 | 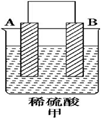 |  | 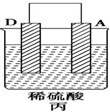 |
| 部分实验现象 | A(二价金属)不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中负极的电极反应为A-2e-═A2+.
②装置乙中正极的电极反应为Cu2++2e-═Cu.
③装置丙中溶液的pH增大(填“增大”、“减小”或“不变”).
④四种金属活动性由强到弱的顺序为D>A>B>C.
(2)在一定温度下,反应2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)达到平衡状态时,n(SO2):n(O2):n (SO3)=2:3:4.缩小体积,再次达到平衡状态时,n(O2)=0.8mol,n(SO3)=1.4mol,下列说法正确的是AB.
A.再次达到平衡状态时,n(SO2)为0.4mol B.缩小体积,再次达到平衡过程中,v正>v逆
C.使用催化剂对反应速率影响不大 D.工业上一般采用增加SO2的浓度来提高O2的转化率.
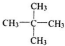 和
和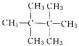 (写结构简式)
(写结构简式)