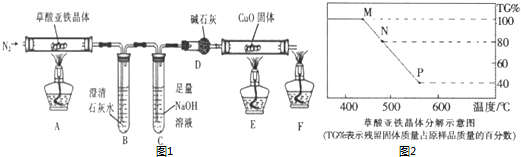
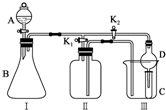
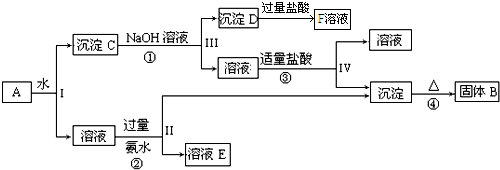
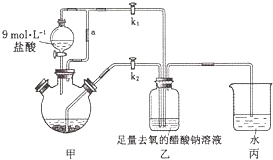
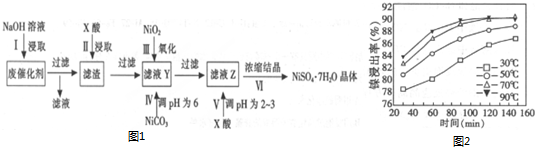
20.某油脂化工厂的含镍废催化剂主要含有Ni,还含有Al、Fe的单质及氧化物,其他是不溶杂质.现用该废催化剂制取NiSO4•7H2O,流程如图1:
部分阳离子以氢氧物形式完全沉淀时的pH如下:
回答下列问题:
(1)第1步加入NaOH溶液的目的是除去Al、Al2O3和油脂等杂质.
(2)“酸浸”时所加入的X酸是硫酸(填化学式).保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2,“酸浸”的适宜温度与时间分别是C(填选项字母).
A.30℃、30min B.90℃、150min C.70℃、120min
(3)第V步调pH为2~3的目的是(请结合化学用语和平衡移动原理解释)溶液中存在水解平衡Ni2++2H2O?Ni(OH)2+2H+,增大氢离子浓度平衡逆向进行避免浓缩过程中水解生成沉淀.
(4)工业上以铝和NiOOH为电极,NaOH溶液为电解液制成电池.放电时,NiOOH转化为Ni(OH)2,该电池正极反应式是NiO(OH)+H2O+e-═Ni(OH)2+OH-.
(5)已知:2Mg(s)+O2(g)=2Mg(s)△H1=-2075kJ/mol
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)△H2=+84.6kJ/mol
MgH2(s)+$\frac{1}{2}$O2(g)=MgO(s)+H2(g)△H3=-963kJ/mol
含镍储氢材料(Mg2NiH4)释放氢气和Mg2Ni的热化学方程式是Mg2NiH4(s)=Mg2Ni(s)+2H2(g)△H=+64.4KJ/mol.
(6)在含镍废催化剂中,Ni、Al和Fe的质量分数分别是29.5%、31%和5.6%.a kg含镍废催化剂按上述流程转化,第Ⅱ步加入cmol/L的X酸bL,酸浸后的滤液Y不含Fe3+,滤液Z中残留的酸忽略不计,则第Ⅳ步应加入NiCO30.119(cb-5.5a)kg.

部分阳离子以氢氧物形式完全沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(1)第1步加入NaOH溶液的目的是除去Al、Al2O3和油脂等杂质.
(2)“酸浸”时所加入的X酸是硫酸(填化学式).保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2,“酸浸”的适宜温度与时间分别是C(填选项字母).
A.30℃、30min B.90℃、150min C.70℃、120min
(3)第V步调pH为2~3的目的是(请结合化学用语和平衡移动原理解释)溶液中存在水解平衡Ni2++2H2O?Ni(OH)2+2H+,增大氢离子浓度平衡逆向进行避免浓缩过程中水解生成沉淀.
(4)工业上以铝和NiOOH为电极,NaOH溶液为电解液制成电池.放电时,NiOOH转化为Ni(OH)2,该电池正极反应式是NiO(OH)+H2O+e-═Ni(OH)2+OH-.
(5)已知:2Mg(s)+O2(g)=2Mg(s)△H1=-2075kJ/mol
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)△H2=+84.6kJ/mol
MgH2(s)+$\frac{1}{2}$O2(g)=MgO(s)+H2(g)△H3=-963kJ/mol
含镍储氢材料(Mg2NiH4)释放氢气和Mg2Ni的热化学方程式是Mg2NiH4(s)=Mg2Ni(s)+2H2(g)△H=+64.4KJ/mol.
(6)在含镍废催化剂中,Ni、Al和Fe的质量分数分别是29.5%、31%和5.6%.a kg含镍废催化剂按上述流程转化,第Ⅱ步加入cmol/L的X酸bL,酸浸后的滤液Y不含Fe3+,滤液Z中残留的酸忽略不计,则第Ⅳ步应加入NiCO30.119(cb-5.5a)kg.
17.在H2与Cl2生成HCl的反应中,已知H-H键、Cl-Cl、和H-Cl键的键能分别为akJ/mol、bkJ/mol、ckJ/mol,则生成1molHCl放出的能量为( )
| A. | (c-a-b)kJ | B. | (a+b-c)kJ | C. | (2c-a-b)kJ | D. | $\frac{2c-a-b}{2}$kJ |
14.用标准浓度的盐酸来滴定未知浓度的NaOH溶液,下列操作会引起测定结果偏低的是( )
| A. | 酸碱中和滴定时,用待测液润洗锥形瓶 | |
| B. | 酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液 | |
| C. | 滴定终点读数时,俯视滴定管的刻度,其他操作正确 | |
| D. | 酸式滴定管尖嘴部分开始实验时有气泡,滴定后无气泡 |
13.实验室现有3种酸碱指示剂,其pH变色范围是:甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0,用0.1 000mol•L-1 NaOH 溶液滴定未知浓度的CH3COOH 溶液,反应恰好完全时,下列叙述中正确的是( )
| A. | 溶液呈中性,可选用甲基橙或酚酞作指示剂 | |
| B. | 溶液呈中性,只能选用石蕊作指示剂 | |
| C. | 溶液呈碱性,可选用甲基橙或酚酞作指示剂 | |
| D. | 溶液呈碱性,只能选用酚酞作指示剂 |
12. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,用标准溶液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液由红色变为无色,且半分钟不再改变时,达到滴定终点.
(2)该小组在步骤①中的错误是锥形瓶不能用待测液润洗
由此造成的测定结果偏高(偏高、偏低或无影响)
(3)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)请根据下表数据计算待测烧碱溶液的浓度0.0800mol/L.
0 155339 155347 155353 155357 155363 155365 155369 155375 155377 155383 155389 155393 155395 155399 155405 155407 155413 155417 155419 155423 155425 155429 155431 155433 155434 155435 155437 155438 155439 155441 155443 155447 155449 155453 155455 155459 155465 155467 155473 155477 155479 155483 155489 155495 155497 155503 155507 155509 155515 155519 155525 155533 203614
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,用标准溶液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液由红色变为无色,且半分钟不再改变时,达到滴定终点.
(2)该小组在步骤①中的错误是锥形瓶不能用待测液润洗
由此造成的测定结果偏高(偏高、偏低或无影响)
(3)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)请根据下表数据计算待测烧碱溶液的浓度0.0800mol/L.
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前度数(mL) | 滴定后度数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |