7.有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是( )
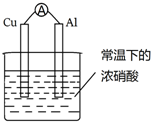

| A. | Cu是原电池的负极 | |
| B. | 电流由Cu电极流出 | |
| C. | 电子由Al沿导线流向Cu | |
| D. | 铝片上的电极反应式为:Al-3e-═Al3+ |
5.有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是( )
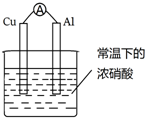

| A. | 电子由Al沿导线流向Cu | |
| B. | 电流由Cu电极流出 | |
| C. | Cu是原电池的负极 | |
| D. | 铝片上的电极反应式为:Al-3e-═Al3+ |
4.在同温同压下,下列各组热化学方程式中△H1>△H2的是( )
| A. | 2H2(g)+O2(g)=2H2O(l)△H1; 2H2(g)+O2(g)=2H2O(g)△H2 | |
| B. | S(g)+O2(g)=SO2(g)△H1; S(s)+O2(g)=SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H1; C(s)+O2(g)=CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g)△H1; $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g)△H2 |
3.下列有关热化学方程式的表示及说法正确的是( )
| A. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol | |
| B. | 含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+$\frac{1}{2}$H2SO4 (aq)=NaCl(aq)+H2O(l)△H=-57.4kJ/mol | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 已知I2(g)+H2(g)=2HI(g)△H1<0;I2(s)+H2(g)=2HI(g )△H2<0,则△H1>△H2 |
2.下列热化学方程式表达正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol (反应热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=+116.2kJ/mol (反应热) |
1.已知:①2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列说法中错误的是( )
②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列说法中错误的是( )
| A. | ①式表示常温常压时,2 mol H2和1 mol O2完全燃烧生成2 mol H2O(l)放热571.6 kJ | |
| B. | 2H2(g)+O2(g)=2H2O(g)中△H大于-571.6 kJ•mol-1 | |
| C. | 将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量大于57.3 kJ | |
| D. | 将含1 mol NaOH的稀溶液与含1 mol CH3COOH的稀溶液混合后放出的热量为57.3 kJ |
20.下列关于反应能量的说法正确的是( )
0 155322 155330 155336 155340 155346 155348 155352 155358 155360 155366 155372 155376 155378 155382 155388 155390 155396 155400 155402 155406 155408 155412 155414 155416 155417 155418 155420 155421 155422 155424 155426 155430 155432 155436 155438 155442 155448 155450 155456 155460 155462 155466 155472 155478 155480 155486 155490 155492 155498 155502 155508 155516 203614
| A. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol 氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量>生成物总能量 |
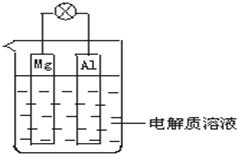 如图所示,试回答下列问题 (灯泡功率合适):
如图所示,试回答下列问题 (灯泡功率合适):

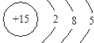 、其最高价氧化物对应的水化物的化学式H3PO4.
、其最高价氧化物对应的水化物的化学式H3PO4.