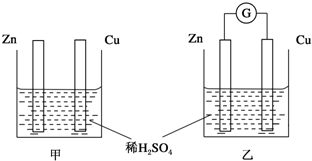
18.下列理解不正确的是( )
| A. | 化学平衡是一个动态平衡 | |
| B. | 化学平衡研究的对象主要是可逆反应 | |
| C. | 化学反应速率是研究化学反应进行的快慢问题,化学平衡是研究化学反应进行的限度问题 | |
| D. | 化学反应达到平衡时,正反应和逆反应速率相等,是对反应中不同物质而言 |
17.下列有机物的系统命名正确的是( )
| A. |  :3-甲基-2-戊烯 :3-甲基-2-戊烯 | B. |  :2-甲基-3-丁炔 :2-甲基-3-丁炔 | ||
| C. |  :1,3,4-三甲苯 :1,3,4-三甲苯 | D. | 2,3-二甲基-2-乙基己烷 |
16.表是元素周期表的一部分.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)画出原子结构示意图:⑪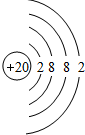 .
.
(5)用电子式表示⑦和⑩形成化合物的过程: .
.
(6)⑦和⑧分别形成的气态氢化物的化学式是H2S、HCl.其中相对不稳定的是H2S.
(7)在③与④中,化学性质较活泼的是Na(填元素符号),在⑧与⑫中,化学性质较活泼的是Cl,(填元素符号)如何证明(用离子方程式表示):Cl2+2Br-═Br2+2Cl-.
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)画出原子结构示意图:⑪
 .
.(5)用电子式表示⑦和⑩形成化合物的过程:
 .
.(6)⑦和⑧分别形成的气态氢化物的化学式是H2S、HCl.其中相对不稳定的是H2S.
(7)在③与④中,化学性质较活泼的是Na(填元素符号),在⑧与⑫中,化学性质较活泼的是Cl,(填元素符号)如何证明(用离子方程式表示):Cl2+2Br-═Br2+2Cl-.
15.化学键是一种作用力,下列不属于化学键的是( )
| A. | 离子键 | B. | 氢键 | C. | 极性共价键 | D. | 非极性共价键 |
14.钾和钠的化学性质相似,下列说法中能最好的解释这个事实的是( )
| A. | 都是金属元素 | B. | 原子半径相差不大 | ||
| C. | 原子的最外层电子数相同 | D. | 最高化合价相同 |
13.用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车.反应的方程式为:2CrO3+3CH3CH2OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O,此反应的氧化剂是( )
| A. | H2SO4 | B. | CrO3 | C. | Cr2(SO4)3 | D. | CH3CH2OH |
11.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色.下列判断正确的是( )
| A. | 金属性:Y>Z | B. | 氢化物的稳定性:X>W | ||
| C. | 离子的还原性:X>W | D. | 离子半径:Z>Y>X |
10.现有部分前四周期元素的性质或原子结构如表:
(1)写出元素E+基态原子的电子排布式:1s22s22p63s23p63d10.
(2)ABCD四种元素电负性由大到小排列顺序为(用元素符号表示)O>N>C>Si
(3)B单质分子中,含有σ键和π键的个数比是1:2,元素C的气态氢化物的杂化方式和空间构型分别为sp3、V形.
(4)以上元素组成的化合物中心原子是sp杂化方式的是CO2(化学式)
(5)A、B、C、D第一电离由大到小的顺序为(用元素符号表示):N>O>C>Si.
0 155319 155327 155333 155337 155343 155345 155349 155355 155357 155363 155369 155373 155375 155379 155385 155387 155393 155397 155399 155403 155405 155409 155411 155413 155414 155415 155417 155418 155419 155421 155423 155427 155429 155433 155435 155439 155445 155447 155453 155457 155459 155463 155469 155475 155477 155483 155487 155489 155495 155499 155505 155513 203614
| 元素编号 | 元素性质或原子结构 |
| A | 第二周期中形成化合物最最多的元素 |
| B | L层s电子数比p电子数少l |
| C | 地壳中含量最高的元素 |
| D | 第三周期中可以作为半导体材料的元素 |
| E | 第四周期中最外层只有一个电子且内层完全排满电子的元素 |
(2)ABCD四种元素电负性由大到小排列顺序为(用元素符号表示)O>N>C>Si
(3)B单质分子中,含有σ键和π键的个数比是1:2,元素C的气态氢化物的杂化方式和空间构型分别为sp3、V形.
(4)以上元素组成的化合物中心原子是sp杂化方式的是CO2(化学式)
(5)A、B、C、D第一电离由大到小的顺序为(用元素符号表示):N>O>C>Si.