19.四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)元素Z位于周期表中第三周期,VA族;
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)Y的最高价氧化物的化学式为N2O5.
请回答下列问题:
| X | Y | |
| Z | W |
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)Y的最高价氧化物的化学式为N2O5.
18.对下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
| A. | 在25℃100 mL NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3•H2O) | |
| B. | 0.1 mol/L的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| C. | 将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 0.1 mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
16.将如图所示实验装置的 K 闭合,下列判断正确的是( )
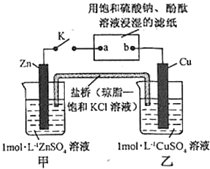

| A. | Cu 电极上发生还原反应 | B. | 电子沿 Zn→a→b→Cu 路径流动 | ||
| C. | 片刻后甲池中 c(SO42-)增大 | D. | 片刻后可观察到滤纸 b 点变红色 |
13.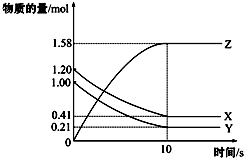 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )| A. | 反应开始到10 s,用Z表示的反应速率为0.158 mol/(L•s) | |
| B. | 反应开始到10 s,X的物质的量浓度减少了0.79 mol/L | |
| C. | 反应开始到10 s时,Y的转化率为79.0% | |
| D. | 在前10 s内用X、Y、Z表示的反应速率数值相等 |
12.某原电池总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的正确组成是( )
| A | B | C | D | |
| 正极 | Zn | Cu | Cu | Fe |
| 负极 | Cu | Zn | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | AgNO3 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法正确的是( )
| A. | 非极性分子中的原子一定无孤电子对 | |
| B. | 平面三角型分子一定是非极性分子 | |
| C. | 二氯甲烷(CH2Cl2)分子的中心原子是SP3杂化,键角均为109°28′ | |
| D. | ABn型分子的中心原子最外层满足8电子结构,则ABn不一定是非极性分子 |
10.下列结论合理的是( )
0 155317 155325 155331 155335 155341 155343 155347 155353 155355 155361 155367 155371 155373 155377 155383 155385 155391 155395 155397 155401 155403 155407 155409 155411 155412 155413 155415 155416 155417 155419 155421 155425 155427 155431 155433 155437 155443 155445 155451 155455 155457 155461 155467 155473 155475 155481 155485 155487 155493 155497 155503 155511 203614
| A. | CH4的稳定性高于SiH4,可推测CH4的沸点也高于SiH4 | |
| B. | 氯化钠的晶格能比氯化铯的晶格能小 | |
| C. | 根据价电子构型与化合价的关系,推出最外层电子数3个的元素一定是第ⅢA族元素 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出SO2通入NaClO溶液中能生成HClO |
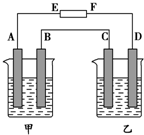 如图中,甲烧杯中盛有100mL 0.50mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则
如图中,甲烧杯中盛有100mL 0.50mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则