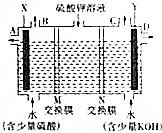
17.如图是H2与Cl2发生反应生成HCl和三个状态的能量,有关说法错误的是( )
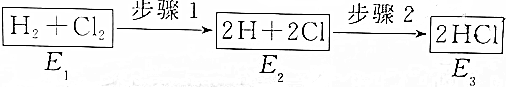
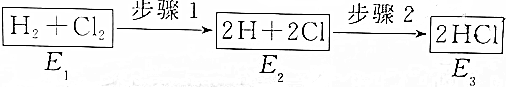
| A. | 步骤2是放热反应 | B. | 三个状态的能量E2最大 | ||
| C. | 要实现步骤1的转化,必须加热 | D. | 该反应放出的热量为E1一E3 |
16.下图是CH4、CCl4、CH3Cl的分子球棍模型图,下列说法正确的是( )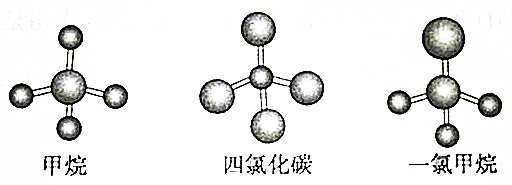

| A. | CH4、CCl4和CH3Cl都是正四面体结构 | |
| B. | CH4、CCl4都是正四面体结构 | |
| C. | CH4和CCl4中的化学键均为非极性键 | |
| D. | CH4、CCl4的结构相同,性质也相同 |
11.已知某元素的阳离子R2+的核内中子数为n,质量数为A,则mg它的氧化物中所含电子的物质的量是( )
| A. | $\frac{m}{A+16}$(A-n+8)mol | B. | $\frac{m}{A+16}$(A-n+10)mol | C. | (A-n+2)mol | D. | $\frac{m}{A}$(A-n+6)mol |
10. 短周期元素A、B、C、D、E原子序数依次增大.A是周期表中原子半径最小的元素,B原子的最外层电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数.
短周期元素A、B、C、D、E原子序数依次增大.A是周期表中原子半径最小的元素,B原子的最外层电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数.
(1)A、C、D形成的化合物中含有的化学键类型为离子键、共价键.
(2)已知:①E-E→2E•;△H=+a kJ•mol-1
②2A•→A-A;△H=-b kJ•mol-1
③E•+A•→A-E;△H=-c kJ•mol-1(“•”表示形成共价键所提供的电子)写出298K时,A2与E2反应的热化学方程式(用化学式表示)H2(g)+Cl2(g)=2HCl(g)△H=(a+b-2c) kJ•mol-1.
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)?X(g);△H=-d kJ•mol-1(d>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
①在该温度下,假设甲容器从反应开始到平衡所需时间为4min,则该时间段内A2的平均反应速率v(A2)=0.125mol/(L.min).
②该温度下此反应的平衡常数K的值为4.
③三个容器中的反应分别达平衡时各组数据关系正确的是ADE(填序号).
A.α1+α2=1 B.α3<α1 C. n2<n3<1.0mol
D.P3<2P1=2P2 E. Q1+Q2=d F.Q3=2Q1
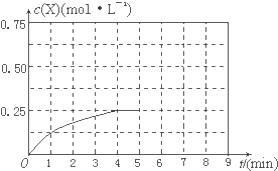
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在图中画出第5min 到新平衡时X的物质的量浓度的变化曲线.
0 155310 155318 155324 155328 155334 155336 155340 155346 155348 155354 155360 155364 155366 155370 155376 155378 155384 155388 155390 155394 155396 155400 155402 155404 155405 155406 155408 155409 155410 155412 155414 155418 155420 155424 155426 155430 155436 155438 155444 155448 155450 155454 155460 155466 155468 155474 155478 155480 155486 155490 155496 155504 203614
 短周期元素A、B、C、D、E原子序数依次增大.A是周期表中原子半径最小的元素,B原子的最外层电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数.
短周期元素A、B、C、D、E原子序数依次增大.A是周期表中原子半径最小的元素,B原子的最外层电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数.(1)A、C、D形成的化合物中含有的化学键类型为离子键、共价键.
(2)已知:①E-E→2E•;△H=+a kJ•mol-1
②2A•→A-A;△H=-b kJ•mol-1
③E•+A•→A-E;△H=-c kJ•mol-1(“•”表示形成共价键所提供的电子)写出298K时,A2与E2反应的热化学方程式(用化学式表示)H2(g)+Cl2(g)=2HCl(g)△H=(a+b-2c) kJ•mol-1.
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)?X(g);△H=-d kJ•mol-1(d>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2molA2、1molBC | 1molX | 4molA2、2molBC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | α1 | α2 | α3 |
②该温度下此反应的平衡常数K的值为4.
③三个容器中的反应分别达平衡时各组数据关系正确的是ADE(填序号).
A.α1+α2=1 B.α3<α1 C. n2<n3<1.0mol
D.P3<2P1=2P2 E. Q1+Q2=d F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在图中画出第5min 到新平衡时X的物质的量浓度的变化曲线.
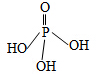 (1)三聚磷酸可视为三个磷酸分子(磷酸的结构如图)之间脱去两个分子的产物,其结构式为
(1)三聚磷酸可视为三个磷酸分子(磷酸的结构如图)之间脱去两个分子的产物,其结构式为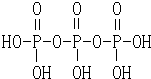 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.