8.一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A. | 若该反应的△H<0,升高温度,平衡常数K减小 | |
| B. | 若增大X的浓度,则物质Y的转化率减小 | |
| C. | 以X浓度变化表示的反应速率为$\frac{1}{8}$ mol/(L•s) | |
| D. | 12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的$\frac{1}{5}$ |
7.下列关于二氧化硅的叙述正确的是( )
①可用于制造光导纤维
②能跟强碱反应,但不能与水反应
③SiO2的物理性质与CO2类似
④既是酸性氧化物,又是碱性氧化物.
①可用于制造光导纤维
②能跟强碱反应,但不能与水反应
③SiO2的物理性质与CO2类似
④既是酸性氧化物,又是碱性氧化物.
| A. | ①和② | B. | ③和④ | C. | ②和④ | D. | ②和③ |
5.已知NaHCO3溶液呈碱性,则下列关系式表示错误的是( )
| A. | c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+) | B. | c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) | ||
| C. | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | D. | c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
4.室温下某溶液中由水电离出的H+浓度为1.0×10-13 mol•L-1,则在此溶液中一定不可能大量存在的离子组是( )
| A. | Al3+、K+、NO3-、Cl- | B. | K+、Na+、HS-、Cl- | ||
| C. | Na+、AlO2-、SO42-、NO3- | D. | Ba2+、Na+、Cl-、NO3- |
3.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石.已知12g石墨完全转化为金刚石时,要吸收a kJ的能量,下列说法正确的是( )
①石墨不如金刚石稳定
②金刚石不如石墨稳定
③等质量的石墨和金刚石完全燃烧,金刚石放出的能量多
④石墨转化为金刚石是氧化还原反应.
①石墨不如金刚石稳定
②金刚石不如石墨稳定
③等质量的石墨和金刚石完全燃烧,金刚石放出的能量多
④石墨转化为金刚石是氧化还原反应.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
2.反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g) 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加Fe(s)的量 | B. | 将容器的体积缩小一半 | ||
| C. | 升高温度 | D. | 通入水蒸气 |
1.下列说法中不正确的是( )
0 155309 155317 155323 155327 155333 155335 155339 155345 155347 155353 155359 155363 155365 155369 155375 155377 155383 155387 155389 155393 155395 155399 155401 155403 155404 155405 155407 155408 155409 155411 155413 155417 155419 155423 155425 155429 155435 155437 155443 155447 155449 155453 155459 155465 155467 155473 155477 155479 155485 155489 155495 155503 203614
| A. | 将化学能转变为电能的装置叫做原电池 | |
| B. | 乙醇和沼气都是可再生能源 | |
| C. | CO2是造成酸雨的主要原因之一 | |
| D. | 质子数相同而中子数不同的同一元素的不同原子互称为同位素 |

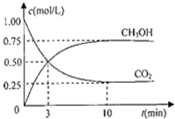 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,