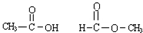16.1999年曾报导合成和分离了含高能量的正离子N5+的化合物N5AsF6,下列叙述错误的是( )
| A. | N5+共有34个核外电子 | |
| B. | N5+中氮氮原子间以共用电子对结合 | |
| C. | 化合物N5AsF6中As化合价为+1 | |
| D. | 化合物N5AsF6属于离子晶体 |
15.已知4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0,下列有关叙述正确的( )
| A. | 上述反应的化学反应速率关系:2 v(NH3)=3 v(H2O) | |
| B. | 若在2L的密闭容器中反应,经过3min后NH3的物质的量由10mol变为7mol则v (NH3)=0.5mol•L-1•s-1 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 若降低温度,反应速率将会减小 |
14.在一定温度下,可逆反应A2(g)+B2(g)═2AB(g)达到化学平衡的标志是 ( )
| A. | 容器内气体的总质量不随时间而变化 | |
| B. | 单位时间内有nmolA2生成的同时就有nmolB2生成 | |
| C. | 2 v(A2)正=v(AB)逆 | |
| D. | A2、B2(g)、AB(g)的浓度之比为1:1:2 |
13.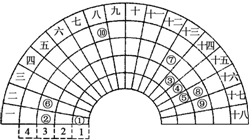 元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
 元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,下图是扇形元素周期表前四周期的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A. | ②、⑧、⑨对应原子半径依次增大 | |
| B. | ②、⑨的氢化物晶体类型相同 | |
| C. | 元素⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ①、③、④、⑤形成的某种化合物中既含有共价键又含有离子键 |
11.已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | +1 | -4 | -2 | -1 |
| A. | 乙的常见氧化物只有一种 | |
| B. | 气态氢化物稳定性:丙>丁 | |
| C. | 原子半径大小:戊<丙 | |
| D. | 丙的氧化物能与戊的氢化物的水溶液反应 |
10.日常所用干电池其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入),电极反应可简化为:Zn-2e-═Zn2+,2NH4++2e-═2NH3↑+H2↑(NH3与Zn2+结合).根据上述叙述判断下列说法中不正确的是( )
| A. | 溶液中 Cl- 移向正极 | |
| B. | 工作时,电流由碳极经外电路流向Zn极 | |
| C. | Zn为负极,碳为正极 | |
| D. | 长时间连续使用时,内装糊状物可能流出腐蚀电器 |
9.下列各组顺序的排列不正确的是( )
0 155308 155316 155322 155326 155332 155334 155338 155344 155346 155352 155358 155362 155364 155368 155374 155376 155382 155386 155388 155392 155394 155398 155400 155402 155403 155404 155406 155407 155408 155410 155412 155416 155418 155422 155424 155428 155434 155436 155442 155446 155448 155452 155458 155464 155466 155472 155476 155478 155484 155488 155494 155502 203614
| A. | 原子半径:F>Na>Mg>Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2CO3<H3PO4<H2SO4 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
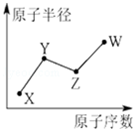 U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示:
U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示: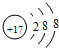 ;
; ;
;