18.以下各反应中,生成物的总能量高于反应物的总能量的是( )
| A. | 甲烷燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 铝片与盐酸反应 | D. | 氧化钙与水反应 |
16.按要求回答下列问题.
(1)A元素的负一价离子的电子层结构与氩相同,它在元素周期表中的位置为第三周期第VIIA族
(2)B元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素名称为碳或氧
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的最外层电子排布式
为4s1
(4)X元素的原子最外层电子排布式为nsnnpn+1,Y元素的某同位素原子无中子.X和Y形成的最简单化合物的结构式为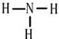
(5)M元素的正三价离子的3d能级为半充满,M基态原子的电子排布式为1s22s22p63s23p63d64s2
(6)如表是N逐级失去电子的电离能.
则元素N的常见价态是+3价.
(1)A元素的负一价离子的电子层结构与氩相同,它在元素周期表中的位置为第三周期第VIIA族
(2)B元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素名称为碳或氧
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的最外层电子排布式
为4s1
(4)X元素的原子最外层电子排布式为nsnnpn+1,Y元素的某同位素原子无中子.X和Y形成的最简单化合物的结构式为
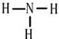
(5)M元素的正三价离子的3d能级为半充满,M基态原子的电子排布式为1s22s22p63s23p63d64s2
(6)如表是N逐级失去电子的电离能.
| I1 | I2 | I3 | I4 | I5 | I6 | |
| In | 578 | 1817 | 2745 | 11578 | 14831 | 18378 |
15.表为元素周期表的一部分,用元素符号或化学用语回答下列问题.
(1)10种元素中,化学性质最不活泼的是Ar,除⑩外原子半径最大的是K
(2)①、②、④、⑧四种元素形成的离子半径由大到小的顺序为Cl->K+>Na+>Al3+,
(3)⑥和高价态的⑤形成的化合物的电子式是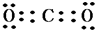 ,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为
,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为 ;用电子式表示元素③和⑨形成化合物的过程
;用电子式表示元素③和⑨形成化合物的过程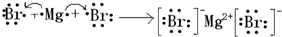
(4)⑥、⑦两种元素形成的简单氢化物中,沸点高的是H2O,原因是水分子之间存在氢键
(5)④和⑧两种元素最高价氧化物对应水化物相互反应的离子方程式3H++Al(OH)3=3H2O+Al3+
(6)写出一个能表示⑦、⑧两种元素非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓,
(7)下列叙述中,肯定a金属比b金属活泼性强的是D(填序号)
A.a原子的最外层电子数比b原子的最外层电子数少
B.a原子的电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比1mol b从酸中置换H+生成的H2多
D.常温时,a能从水中置换出氢,而b不能.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ⑨ |
(2)①、②、④、⑧四种元素形成的离子半径由大到小的顺序为Cl->K+>Na+>Al3+,
(3)⑥和高价态的⑤形成的化合物的电子式是
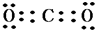 ,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为
,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为 ;用电子式表示元素③和⑨形成化合物的过程
;用电子式表示元素③和⑨形成化合物的过程
(4)⑥、⑦两种元素形成的简单氢化物中,沸点高的是H2O,原因是水分子之间存在氢键
(5)④和⑧两种元素最高价氧化物对应水化物相互反应的离子方程式3H++Al(OH)3=3H2O+Al3+
(6)写出一个能表示⑦、⑧两种元素非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓,
(7)下列叙述中,肯定a金属比b金属活泼性强的是D(填序号)
A.a原子的最外层电子数比b原子的最外层电子数少
B.a原子的电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比1mol b从酸中置换H+生成的H2多
D.常温时,a能从水中置换出氢,而b不能.
14.如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )


| A. | WX3和水反应形成的化合物是共价化合物 | |
| B. | 单质的熔点:Y>Z | |
| C. | X、Y、R形成的某种化合物可以用于漂白、消毒 | |
| D. | Y、Z和W三者最高价氧化物对应的水化物能两两相互反应 |
13.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | 气态氢化物的稳定性:Y>W>X | |
| B. | X、Y两种元素形成的化合物只有两种 | |
| C. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
12.下列现象与化学键有关的是( )
| A. | H2O在高温下也难分解 | |
| B. | F2、Cl2、Br2、I2单质的熔点依次升高 | |
| C. | SiH4的熔点高于CH4的熔点 | |
| D. | NH3的沸点高于PH3的沸点 |
11.短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13.X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素.下列说法正确的是( )
| A. | Y2分子中,σ键和π键数目之比为2:1 | |
| B. | Z单质与W单质发生反应,产物只有一种 | |
| C. | 元素X、Z形成的化合物中仅含极性共价键 | |
| D. | 只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
9.短周期元素X、Y、Z、W、Q在表中的位置如图所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是( )
0 155294 155302 155308 155312 155318 155320 155324 155330 155332 155338 155344 155348 155350 155354 155360 155362 155368 155372 155374 155378 155380 155384 155386 155388 155389 155390 155392 155393 155394 155396 155398 155402 155404 155408 155410 155414 155420 155422 155428 155432 155434 155438 155444 155450 155452 155458 155462 155464 155470 155474 155480 155488 203614
| X | Y | ||
| Z | W | Q |
| A. | 钠与W可以形成离子化合物Na2W2 | |
| B. | 由Z与Y组成的物质在熔融时能导电 | |
| C. | 氧化物对应水化物的酸性:Q>W | |
| D. | 固态XY2和ZY2的化学键类型、晶体类型都相同 |