8.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有6个电子,Y是至今发现的非金属性最强的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料.下列叙述不正确的是( )
| A. | 原子最外层电子数:Y>X>W>Z | B. | 原子半径:Z>W>X>Y | ||
| C. | 电负性:Y>X>W>Z | D. | 简单气态氢化物的沸点:Y>X |
7.下列各组指定的元素,不能形成AB2型共价化合物的是( )
| A. | 2s22p2和2s22p4 | B. | 3s23p4和2s22p2 | C. | 3s2和3s23p5 | D. | 2s22p3和2s22p4 |
6.W、X、Y、Z是短周期元素,其部分性质如下表:
下列说法不正确的是( )
| 元素 | 部 分 性 质 |
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是核外电子总数的$\frac{7}{17}$ |
| Z | 第三周期原子半径最小的金属 |
| A. | 第一电离能:Y>Z | |
| B. | 离子半径:W>Z | |
| C. | X、Y形成的化合物XY4是离子化合物 | |
| D. | 工业上利用电解熔融Z的氧化物生产Z金属单质 |
5.下列实验事实:
①常温下S为固体,而Cl2为气体;
②Cl2与H2混合,强光照射剧烈反应,而S与H2反应需较高温度;
③Cl2与Fe反应,Cl2生成FeCl3,而S与Fe生成FeS;
④盐酸是强酸,而氢硫酸是弱酸;
⑤将Cl2通入氢硫酸中可置换出S
能说明Cl的非金属性比S强的事实有( )
①常温下S为固体,而Cl2为气体;
②Cl2与H2混合,强光照射剧烈反应,而S与H2反应需较高温度;
③Cl2与Fe反应,Cl2生成FeCl3,而S与Fe生成FeS;
④盐酸是强酸,而氢硫酸是弱酸;
⑤将Cl2通入氢硫酸中可置换出S
能说明Cl的非金属性比S强的事实有( )
| A. | ①③⑤ | B. | ②③④ | C. | ②③⑤ | D. | ②③④⑤ |
4.已知W、X、Y、Z是短周期元素,aW3+、bX+、cY2-、dZ-四种离子具有相同的电子层结构,下列关系正确的是( )
| A. | 最外层电子数:Y>Z | |
| B. | 核电荷数:a>b | |
| C. | 稳定性:H2Y>HZ | |
| D. | X单质一定能从W的盐溶液中置换出W单质 |
3.下列叙述正确的是( )
| A. | 同一周期元素的原子,半径越小越容易失去电子 | |
| B. | 元素的性质呈周期性变化的根本原因是核外电子排布呈周期性变化 | |
| C. | 第IA族元素与第VIIA族元素形成的化合物都是离子化合物 | |
| D. | 元素周期表中所有元素都是从自然界中发现的,过渡元素都是金属元素 |
2.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p2; ②1s22s22p63s23p4; ③1s22s22p5
则下列有关比较中不正确的是( )
则下列有关比较中不正确的是( )
| A. | 最高正化合价:③>②>① | B. | 原子半径:①>②>③ | ||
| C. | 电负性:③>②>① | D. | 第一电离能:③>②>① |
1.下列各组物质发生变化时,所克服的微粒间作用力属于同种类型的是( )
| A. | 二氧化硅和氢氧化钠的熔化 | B. | 碘和干冰的升华 | ||
| C. | 氯化氢和氯化钠的溶解 | D. | 汞和硫的气化 |
20.下列物质中,含有共价键的离子晶体是( )
| A. | MgCl2 | B. | SO2 | C. | I2 | D. | NaOH |
19.下列化学用语表述正确的是( )
0 155293 155301 155307 155311 155317 155319 155323 155329 155331 155337 155343 155347 155349 155353 155359 155361 155367 155371 155373 155377 155379 155383 155385 155387 155388 155389 155391 155392 155393 155395 155397 155401 155403 155407 155409 155413 155419 155421 155427 155431 155433 155437 155443 155449 155451 155457 155461 155463 155469 155473 155479 155487 203614
| A. | ${\;}_{8}^{16}$O2-的结构示意图: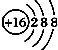 | |
| B. | NH4Br的电子式: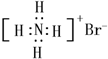 | |
| C. | CCl4的结构式 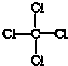 | |
| D. | 氧元素基态原子的电子排布式:1s22s12p3 |