18.通过14C标记的C60进行跟踪研究,医学界发现了一种C60的羧酸衍生物在特定的条件下可通过断裂DNA杀死艾滋病病毒.有关C60和14C的叙述正确的是( )
| A. | 12C60与14C60互为同位素 | |
| B. | 14C转变为12C的过程属于化学变化 | |
| C. | 12C与14C的原子中含有的中子数之比为3:4 | |
| D. | 金刚石与C60都属于原子晶体 |
17.标准状况下,在干燥的烧瓶中充满纯净的NH3进行如图所示的喷泉实验下列说法错误的是( )


| A. | 若烧瓶的氨气中混有少量氮气,则喷泉实验后的水不能充满烧瓶 | |
| B. | 本实验之所以能够产生喷泉是因为氨气极易溶于水,导致烧瓶内外存在压强差 | |
| C. | 本实验若将NH3换成Cl2,烧杯中水换成饱和食盐水,也能产生喷泉 | |
| D. | 实验结束后烧瓶中氨水的物质的量浓度为$\frac{1}{22.4}$ mol•L-1 |
16.工业上制备硫酸常用接触法,工业上制硝酸常用氨的催化氧化法.下列关于工业上制硫酸与硝酸的说法中不正确的是( )
| A. | 在沸腾炉中进行的反应为:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2 | |
| B. | 制硫酸在吸收塔中是用水来吸收SO3 | |
| C. | 氨催化氧化制硝酸过程中的三个主要反应都属于氧化还原反应 | |
| D. | 硫酸工业、硝酸工业都需要对工业尾气进行处理 |
14.废弃物资源化对于建设资源节约型社会具有重要的意义.研究小组测某矿灰的成分,其主要成分为Fe,可能还含有KCl、FeO、Fe2O3、MgO、SiO2、MnO2中的若干种.为了确认其成分,某同学依次进行了以下实验:
①将过量的稀盐酸加入矿灰中,充分反应后过滤得到溶液甲和固体乙
②取少量溶液甲滴加AgNO3溶液,生成白色沉淀
③取少量溶液甲分成两等份,向其中一份滴加酸性高锰酸钾溶液,高锰酸钾溶液褪色;向另一份滴加KSCN溶液,溶液变成血红色
④取少量溶液甲加入过量NaOH溶液,并置于空气中.充分反应后经过滤、洗涤、灼烧得到1.60g固体丙,将固体丙置于氢气流中加热充分反应后得到1.12g固体丁
根据以上实验现象或数据,该同学得出的结论正确的是( )
①将过量的稀盐酸加入矿灰中,充分反应后过滤得到溶液甲和固体乙
②取少量溶液甲滴加AgNO3溶液,生成白色沉淀
③取少量溶液甲分成两等份,向其中一份滴加酸性高锰酸钾溶液,高锰酸钾溶液褪色;向另一份滴加KSCN溶液,溶液变成血红色
④取少量溶液甲加入过量NaOH溶液,并置于空气中.充分反应后经过滤、洗涤、灼烧得到1.60g固体丙,将固体丙置于氢气流中加热充分反应后得到1.12g固体丁
根据以上实验现象或数据,该同学得出的结论正确的是( )
| A. | 根据①可推出矿灰中一定含有SiO2 | |
| B. | 根据②可推出矿灰中一定含有KCl | |
| C. | 根据③可推出矿灰中一定含有FeO和Fe2O3 | |
| D. | 根据④可推出固体丙中一定不含MgO |
13.下列物质的制备,符合工业生产实际的是( )
| A. | 工业上炼铁时,常用石灰石除去铁矿石中的SiO2 | |
| B. | 工业上用接触法制硫酸,在接触室里制出硫酸 | |
| C. | 工业上用二氧化硅在高温下与焦炭反应制得高纯度的硅 | |
| D. | 工业上主要从海水中提取碘 |
12.表为元素周期表的一部分,X、Y、Z、R为短周期元素,其中Y元素的原子最外层电子数是其内层电子数的3倍.
下列说法正确的是( )
| X | Y | |
| Z | R | |
| W |
| A. | 原子半径大小关系为:R>Y>X | |
| B. | X有多种同素异形体,而Y不存在同素异形体 | |
| C. | 根据元素周期律,可以推测W元素的单质具有半导体特性,W2Y3具有氧化性和还原性 | |
| D. | ZY2晶体熔化、液态RY3气化均需克服分子间作用力 |
11.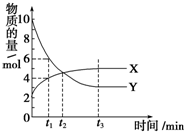 一定温度下在2L密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在2L密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为3X(g)?7Y(g) | |
| B. | t1时,Y的浓度是X浓度的1.5倍 | |
| C. | t2时,正、逆反应速率相等 | |
| D. | 0到t1时间段内,Y的平均反应速率为4/t1 mol•L-1•min-1 |
10.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 同主族元素性质的相似性 | 钠和氧反应可以形成Na2O2,也可以和硫形成Na2S2 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铁片分别加入足量的稀硫酸和浓硫酸中,浓硫酸中铁片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | HF沸点低于HCl |
| D | 较强酸可以制取较弱酸 | 亚硫酸和次氯酸钙反应可以制取次氯酸 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法正确的是( )
0 155292 155300 155306 155310 155316 155318 155322 155328 155330 155336 155342 155346 155348 155352 155358 155360 155366 155370 155372 155376 155378 155382 155384 155386 155387 155388 155390 155391 155392 155394 155396 155400 155402 155406 155408 155412 155418 155420 155426 155430 155432 155436 155442 155448 155450 155456 155460 155462 155468 155472 155478 155486 203614
| A. | 第三周期主族元素从左到右,氧化物对应的水化物酸性依次增强 | |
| B. | H2O比H2S的稳定性强,是因为其分子之间存在氢键 | |
| C. | 金刚石呈正四面体网状结构、C60呈笼状结构,这两种晶体中微粒间的作用力不完全相同 | |
| D. | NH4Cl属于离子化合物,该物质中只存在离子键 |
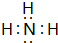 B位于周期表中第二周期ⅦA族.
B位于周期表中第二周期ⅦA族.