2. X、Y、Z、R、T为周期表前四周期的元素,原子序数依次增大.X元素的一种核素无中子存在,Y的2p能级中有1个空轨道,Z的单质为空气的主要成分,R的最外层电子数为其内层电子数的3倍,T原子的价层电排布式是3d74s2.回答下列问题:
X、Y、Z、R、T为周期表前四周期的元素,原子序数依次增大.X元素的一种核素无中子存在,Y的2p能级中有1个空轨道,Z的单质为空气的主要成分,R的最外层电子数为其内层电子数的3倍,T原子的价层电排布式是3d74s2.回答下列问题:
(1)T原子的价层电子排布图是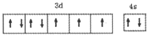 .
.
(2)在Y2X4分子中,Y原子的杂化轨道类型是sp2.
(3)用“<”或“>”填空:
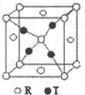
(4)R和T形成的一种离子晶体结构如图,则该晶体中T离子的配位数是4.
(5)TR放入足量的XYZ溶液(呈弱酸性,分解温度1200℃)中,微热产生一种气体单质和[T(YZ)6]3-离子,该反应的离子方程式为2CoO+12HCN=2[Co(CN)6]3-+6H++H2↑+2H2O.
 X、Y、Z、R、T为周期表前四周期的元素,原子序数依次增大.X元素的一种核素无中子存在,Y的2p能级中有1个空轨道,Z的单质为空气的主要成分,R的最外层电子数为其内层电子数的3倍,T原子的价层电排布式是3d74s2.回答下列问题:
X、Y、Z、R、T为周期表前四周期的元素,原子序数依次增大.X元素的一种核素无中子存在,Y的2p能级中有1个空轨道,Z的单质为空气的主要成分,R的最外层电子数为其内层电子数的3倍,T原子的价层电排布式是3d74s2.回答下列问题:(1)T原子的价层电子排布图是
 .
.(2)在Y2X4分子中,Y原子的杂化轨道类型是sp2.
(3)用“<”或“>”填空:
| 电负性 | 原子半径 | 沸点 | 酸性 |
| Y<Z | Z>R | Y2X6<YX4R | XZR3>XZR2 |
(5)TR放入足量的XYZ溶液(呈弱酸性,分解温度1200℃)中,微热产生一种气体单质和[T(YZ)6]3-离子,该反应的离子方程式为2CoO+12HCN=2[Co(CN)6]3-+6H++H2↑+2H2O.
1.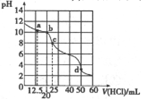 室温下,用0.1000mol/L盐酸滴定25mL0.1000mol/LNa2A溶液(已知H2A为二元弱酸),其滴定曲线如图所示,下列对滴定中所得溶液的相关离子浓度关系判断正确的是( )
室温下,用0.1000mol/L盐酸滴定25mL0.1000mol/LNa2A溶液(已知H2A为二元弱酸),其滴定曲线如图所示,下列对滴定中所得溶液的相关离子浓度关系判断正确的是( )
 室温下,用0.1000mol/L盐酸滴定25mL0.1000mol/LNa2A溶液(已知H2A为二元弱酸),其滴定曲线如图所示,下列对滴定中所得溶液的相关离子浓度关系判断正确的是( )
室温下,用0.1000mol/L盐酸滴定25mL0.1000mol/LNa2A溶液(已知H2A为二元弱酸),其滴定曲线如图所示,下列对滴定中所得溶液的相关离子浓度关系判断正确的是( )| A. | a点:c(A2-)=c(HA-) | B. | b点:5c(Cl-)=4[c(A2-)+c(HA-)+c(H2A)] | ||
| C. | c点:c(Na+)>c(HA-)>c(A2-)>c(H2A) | D. | d点:c(H+)=c(HA-)+c(A2-)+c(OH-) |
20.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LN2中含有π健数为3NA | |
| B. | 12g金刚石中含有C-C键数为4NA | |
| C. | 25℃时,pH=12的CH3COONa溶液中水电离出的OH-的数目为0.01NA | |
| D. | 当反应3(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$4NH3↑+3SO2↑+N2↑+6H2O生成89.6L标准状况的气体时,转移的电子数为3NA |
19. 电解NO制备NH4NO3的工作原理如图所示,为使电解产物全部转化为NH4NO3,通入物质X.下列说法不正确的是( )
电解NO制备NH4NO3的工作原理如图所示,为使电解产物全部转化为NH4NO3,通入物质X.下列说法不正确的是( )
0 155287 155295 155301 155305 155311 155313 155317 155323 155325 155331 155337 155341 155343 155347 155353 155355 155361 155365 155367 155371 155373 155377 155379 155381 155382 155383 155385 155386 155387 155389 155391 155395 155397 155401 155403 155407 155413 155415 155421 155425 155427 155431 155437 155443 155445 155451 155455 155457 155463 155467 155473 155481 203614
 电解NO制备NH4NO3的工作原理如图所示,为使电解产物全部转化为NH4NO3,通入物质X.下列说法不正确的是( )
电解NO制备NH4NO3的工作原理如图所示,为使电解产物全部转化为NH4NO3,通入物质X.下列说法不正确的是( )| A. | a极接电源的负极 | |
| B. | 阳极反应为:NO-3e-+2H2O=NO3-+4H+ | |
| C. | 阴极反应为:NO+5e-+6H+=NH4++H2O | |
| D. | X为NH3最终制得3molNH4NO3理论上需补充2molX物质 |
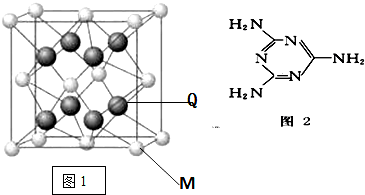
 H、C、N、O、Na、Fe、Cu是常见的七种元素,请回答下列问题:
H、C、N、O、Na、Fe、Cu是常见的七种元素,请回答下列问题: .
.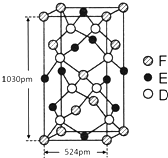 已知A、B、C、D四种短周期元素,它们的核电荷数依次增大.A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族. E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息填空:
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大.A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族. E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息填空: ,F原子的电子排布式是1s22s22p63s23p63d104s1.
,F原子的电子排布式是1s22s22p63s23p63d104s1. .DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.
.DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.
 ;F的结构简式为
;F的结构简式为 .
. .
. )的合成路线
)的合成路线 .
.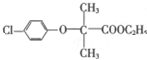 ).
).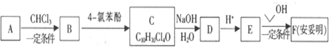
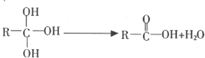 ;
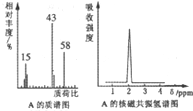
;
 .
. 与O2反应的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
与O2反应的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.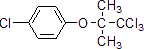 .
.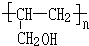 .
.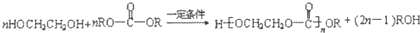
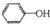 生成中间体N,N与
生成中间体N,N与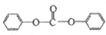 合成工程塑料M(
合成工程塑料M(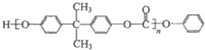 ),则由N合成M的聚合反应方程式为n
),则由N合成M的聚合反应方程式为n +n
+n