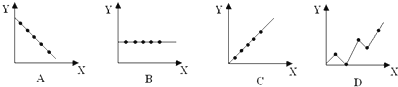
11.对于在密闭容器中进行的可逆反应2SO2(g)+18O2(g)?2SO3(g),下列说法正确的是( )
| A. | 容器内只含有18O2、SO2、SO3三种分子 | |
| B. | 18O只存在18O2分子中 | |
| C. | 容器内含有18O2、S18O2、S18O3等分子 | |
| D. | 反应达到限度时,所有物质的质量都相等 |
7.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定、易分解,CuH在氯气中能燃烧,跟盐酸反应能产生气体,以下有关它的推断中错误的是( )
| A. | “另一种反应物”一定具有还原性 | B. | “另一种反应物”一定只具有氧化性 | ||
| C. | 2CuH+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl | D. | CuH既可作氧化剂也可作还原剂 |
6.短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | W得电子能力比Q强 | |
| B. | Z的氧化物能与水直接化合生成对应的酸 | |
| C. | 钠与Y可能形成的两种常见化合物阴阳离子个数比均为1:2 | |
| D. | X有多种同素异形体,而Y不存在同素异形体 |
5.向以下四种溶液中分别持续通入CO2,最终得到沉淀的一组是( )
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
| A. | ①③④ | B. | ②③④ | C. | ③④ | D. | ①②③ |
4.某元素的一种同位素X的原子质量数为A,含N个中子,它与11H原子组成HmX分子.在a 克HmX中所含质子的物质的量是( )
| A. | $\frac{a}{m+A}$(A-N+m)mol | B. | $\frac{a}{A}$(A一N)mol | C. | $\frac{a}{m+A}$(A-N)mol | D. | $\frac{a}{A}$(A一N+m)mol |
3.下列离子方程式书写正确的是( )
| A. | 用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 水玻璃中加入稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ | |
| C. | 在氯化铝溶液中滴加过量的氨水:Al3++3 OH-═Al (OH)3↓ | |
| D. | 大理石与盐酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
2.下列关于元素周期表的说法正确的是( )
0 155267 155275 155281 155285 155291 155293 155297 155303 155305 155311 155317 155321 155323 155327 155333 155335 155341 155345 155347 155351 155353 155357 155359 155361 155362 155363 155365 155366 155367 155369 155371 155375 155377 155381 155383 155387 155393 155395 155401 155405 155407 155411 155417 155423 155425 155431 155435 155437 155443 155447 155453 155461 203614
| A. | 单质能与水反应生成强碱的金属元素都在ⅠA族 | |
| B. | L层上的电子数为奇数的元素一定是主族元素 | |
| C. | 稀有气体元素原子的最外层电子数均为8 | |
| D. | 元素周期表有18个纵行,分列16个族,即7个主族、8个副族和一个零族 |
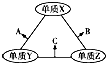 (Ⅰ) W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻; X,Y位于同一主族,它们能组成YX2,YX3两种常见化合物;W元素的氢化物与Z元素的氢化物反应生成盐.请回答下列问题:
(Ⅰ) W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻; X,Y位于同一主族,它们能组成YX2,YX3两种常见化合物;W元素的氢化物与Z元素的氢化物反应生成盐.请回答下列问题: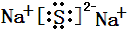 .(用元素符号表示)
.(用元素符号表示)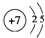 .
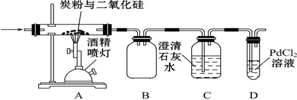
.
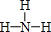 .
.