5.现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
回答下列问题:
(1)③的元素符号是Li;⑧的元素名称是硼;①在元素周期表中的位置是第二周期第VIA族;
(2)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3
(3)用电子式表示②和⑤组成的化合物的形成过程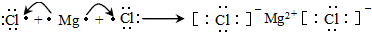 ;
;
(4)写出⑦的最高价氧化物对应的水化物与它的氢化物发生反应的化学方程式NH3+HNO3=NH4NO3
(5)写出②的最高价氧化物对应的水化物跟⑤的氢化物水溶液发生反应的离子方程式Mg(OH)2+2H+=Mg2++2H2O;
(6)“神舟”十号载人飞船内需要一种化合物来吸收航天员呼出的CO2,你认为该物质应该由上表中的①⑥元素组成(填表中编号),用化学方程式表示吸收原理2Na2O2+2CO2=2Na2CO3+O2.
| 编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是Li;⑧的元素名称是硼;①在元素周期表中的位置是第二周期第VIA族;
(2)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3
(3)用电子式表示②和⑤组成的化合物的形成过程
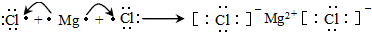 ;
;(4)写出⑦的最高价氧化物对应的水化物与它的氢化物发生反应的化学方程式NH3+HNO3=NH4NO3
(5)写出②的最高价氧化物对应的水化物跟⑤的氢化物水溶液发生反应的离子方程式Mg(OH)2+2H+=Mg2++2H2O;
(6)“神舟”十号载人飞船内需要一种化合物来吸收航天员呼出的CO2,你认为该物质应该由上表中的①⑥元素组成(填表中编号),用化学方程式表示吸收原理2Na2O2+2CO2=2Na2CO3+O2.
3.我国科学家成功地研制出长期依赖进口、价格昂贵的物质${\;}_{8}^{18}$O2.下列说法正确的是( )
| A. | 它是一种新元素 | |
| B. | 它和O3互为同素异形体 | |
| C. | ${\;}_{8}^{18}$O2与${\;}_{2}^{16}$O2互为同位素 | |
| D. | 1mol ${\;}_{8}^{18}$O2分子中含有20mol电子 |
2.下列排序正确的是( )
| A. | 沸点:CH4>NH3 | B. | 原子半径:Na>Mg | C. | 热稳定性:H2S>HF | D. | 还原性:I?<Br? |
1.元素性质的周期性变化不包括( )
0 155248 155256 155262 155266 155272 155274 155278 155284 155286 155292 155298 155302 155304 155308 155314 155316 155322 155326 155328 155332 155334 155338 155340 155342 155343 155344 155346 155347 155348 155350 155352 155356 155358 155362 155364 155368 155374 155376 155382 155386 155388 155392 155398 155404 155406 155412 155416 155418 155424 155428 155434 155442 203614
| A. | 原子半径 | B. | 元素的主要化合价 | ||
| C. | 相对原子质量 | D. | 金属性和非金属性 |
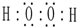 ;肼的结构式
;肼的结构式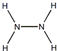 ;
;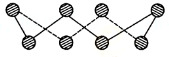 VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化台物在研究和生产中有许多重要用途.请回答下列问题:
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化台物在研究和生产中有许多重要用途.请回答下列问题: