12.元素X和Y的原子序数都小于18,两者能组成化合物XY3.已知X的原子序数为n,则Y 的原子序数不可能是( )
| A. | n+3 | B. | n+4 | C. | n-6 | D. | n-8 |
11.下列说法中正确的是( )
| A. | 在化学键的断裂过程中,肯定发生了化学反应 | |
| B. | 发生能量变化的一定是化学反应 | |
| C. | 离子化合物中一定含有离子键,共价化合物中一定不含离子键 | |
| D. | 在化学键的断裂过程中,肯定放出能量 |
10.用含Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O.工艺流程如下: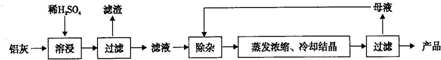
(一定条件下,MnO4-可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的pH
(1)H2SO4溶解Al2O3的离子方程式是Al2O3+6H+=2Al3++3H2O.
(2)检验滤液中还存在Fe2+的方法是取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
Ⅰ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3.2;
Ⅱ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅲ.加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的是将Fe2+氧化为Fe3+;调节溶液的pH为3.2的目的是调节pH值使铁元素沉淀完全.
②向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是有黄绿色气体生成.
③Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式).

(一定条件下,MnO4-可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
(2)检验滤液中还存在Fe2+的方法是取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
Ⅰ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3.2;
Ⅱ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅲ.加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的是将Fe2+氧化为Fe3+;调节溶液的pH为3.2的目的是调节pH值使铁元素沉淀完全.
②向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是有黄绿色气体生成.
③Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式).
9.甲学生对Cl2和FeCl2和KSCN混合溶液的反应进行实验探究.
(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)A中溶液变红的原因是(用离子方程式表示)2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.
甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为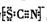 .
.
①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②通过实验证明了SCN- 中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成.
③若SCN-与Cl2反应生成1molCO2,则转移电子的物质的量是16mol.
| 操作 | 现象 |
通入氯气至过量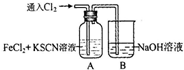 | Ⅰ、A中溶液变红 Ⅱ、稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是(用离子方程式表示)2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.
甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
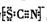 .
.①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②通过实验证明了SCN- 中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成.
③若SCN-与Cl2反应生成1molCO2,则转移电子的物质的量是16mol.
7.氙和氟单质按一定比例混合,在一定条件下反应达到如下平衡:Xe(气)+2F2(气)?XeF4(气)△H=-218kJ/mol,下列措施中既能加快反应速率,又能使平衡向正反应方向移动的是( )
| A. | 升温 | B. | 加压 | C. | 减压 | D. | 降温 |
4.短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子的最外层电子数之和为12,Y、Z、W位于同一周期,Z原子的最外层电子数既是X原子内层电子总数的3倍,又是Y原子最外层电子数的3倍.下列说法正确的是( )
| A. | 原子半径:Y>X,离子半径:Z<W | |
| B. | 元素Y的单质能与元素X的最高价氧化物发生置换反应 | |
| C. | 元素Y和W能形成YW2型共价化合物 | |
| D. | W的单质有毒,且有漂白性 |
3.下列离子组在一定条件下能大量共存,且加入相应试剂后发生反应的离子方程式书写正确的是( )
0 155213 155221 155227 155231 155237 155239 155243 155249 155251 155257 155263 155267 155269 155273 155279 155281 155287 155291 155293 155297 155299 155303 155305 155307 155308 155309 155311 155312 155313 155315 155317 155321 155323 155327 155329 155333 155339 155341 155347 155351 155353 155357 155363 155369 155371 155377 155381 155383 155389 155393 155399 155407 203614
| 选项 | 离子组 | 试剂 | 发生反应的离子方程式 |
| A | K+、AlO2-、NO3- | 过量CO2 | CO2+2H2O+AlO2-=Al(OH)3↓+HCO3- |
| B | Fe3+、I-、ClO- | 少量NaOH溶液 | Fe3++3OH-=Fe(OH) 3↓ |
| C | Ca2+、Na+、OH- | 少量NaHCO3溶液 | HCO3-+OH-=CO32-+H2O |
| D | NH4+、HCO3-、Cl- | 少量NaOH溶液 | NH4++OH-=NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
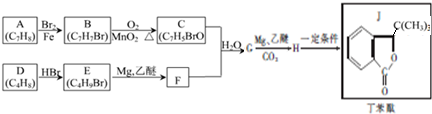
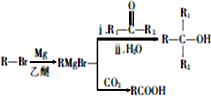
 .
.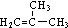 +HBr→(CH3)3CBr.
+HBr→(CH3)3CBr.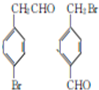 .
. )
) .
.