2.分子式为C7H12O4的酯,在酸性条件下水解生成一种二元有机酸X和一种醇Y,下列有关有机酸X和醇Y的结构数目正确的是( )
| 选项 | 有机酸X的数目 | 醇Y的数目 |
| A | 4种 | 3种 |
| B | 4种 | 2种 |
| C | 5种 | 3种 |
| D | 5种 | 2种 |
| A. | A | B. | B | C. | C | D. | D |
1.化学知识在生产、生活中有着广泛的应用.下列说法中正确的是( )
| A. | 单质硅是将太阳能转变为电能的常用材料 | |
| B. | 制作航天服的聚酯纤维是新型无机非金属材料 | |
| C. | 为了防止食品受潮变质,常在食品包装袋中放入活性铁粉 | |
| D. | 碱性锌锰干电池属于二次电池 |
18.某化工厂利用原电池原理处理废水并淡化海水.工作示意图如下.下列说法正确的是( )

| A. | 电极a在装置中做正极 | |
| B. | 装置中膜A是阳离子交换膜 | |
| C. | 电极b的电极反应式是2NO3-+10e-+12H+═N2↑+6H2O | |
| D. | 若有机物表示为C4H8O2,每转移10mol电子,电极a上产生22.4LCO2(标准状况) |
17.下列实验装置能达到目的是( )
| 选项 | A | B | C | D |
| 装置 | 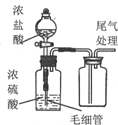 | 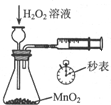 | 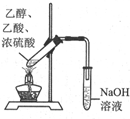 | 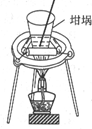 |
| 目的 | 快速制取少量HCl气体 | 测定不同浓度的H2O2溶液对产生O2速率的影响 | 制备并收集乙酸乙酯 | 从小苏打溶液中提取NaHCO3晶体 |
| A. | A | B. | B | C. | C | D. | D |
16.有机化合物9,10-二甲基菲的结构如图所示.其苯环上七氯代物的同分异构体有( )
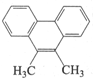

| A. | 8种 | B. | 5种 | C. | 4种 | D. | 3种 |
15.由石英砂(主要含SiO2)制取高纯硅的工业流程如下:下列说法不正确的是( )

| A. | 反应①③均属于置换反应 | |
| B. | 反应①中氧化产物和还原产物的质量比为1:2 | |
| C. | 该流程中反应①③的还原剂不能互换使用 | |
| D. | 该流程是实现半导体工业“从沙滩到用户”的基础 |
14.漂白剂常用于日常生活和工业生产中,下列有关说法正确的是( )
0 155212 155220 155226 155230 155236 155238 155242 155248 155250 155256 155262 155266 155268 155272 155278 155280 155286 155290 155292 155296 155298 155302 155304 155306 155307 155308 155310 155311 155312 155314 155316 155320 155322 155326 155328 155332 155338 155340 155346 155350 155352 155356 155362 155368 155370 155376 155380 155382 155388 155392 155398 155406 203614
| A. | 活性炭与新制氯水的漂白原理相同 | |
| B. | 过氧化钠常用于羽绒制品的漂白 | |
| C. | 漂白粉是由Ca(ClO)2组成的纯净物 | |
| D. | 将漂白剂SO2和NaClO混合使用可增加漂白效果 |
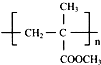 ,以下是有机玻璃的一种合成路线:
,以下是有机玻璃的一种合成路线: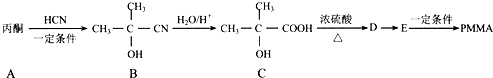
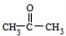 ,A生成B的反应类型是加成反应.
,A生成B的反应类型是加成反应.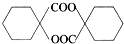 .
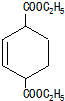
.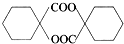 的同分异构体中符合下列条件的有10种(不考虑立体异构);
的同分异构体中符合下列条件的有10种(不考虑立体异构);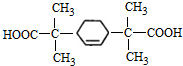 (填结构简式).
(填结构简式).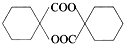 的合成路线:
的合成路线: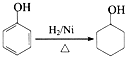 $→_{Cu/△}^{O_{2}}$
$→_{Cu/△}^{O_{2}}$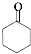 $→_{一定条件}^{HCN}$
$→_{一定条件}^{HCN}$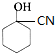 $\stackrel{H_{2}O/H+}{→}$
$\stackrel{H_{2}O/H+}{→}$ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$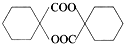 .
.
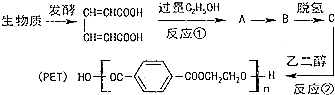
 .
.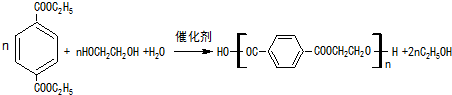 .
.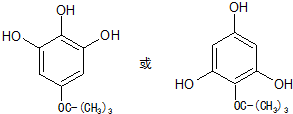 (任写一种)
(任写一种)