15.一定能在下列溶液中大量共存的离子组是( )
| A. | pH=0的溶液:Fe2+、Mg2+、NO3-、SO42- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- | |
| D. | pH=12的溶液:Na+、K+、〔Al(OH)4〕-、CO32- |
14.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| C. | 室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 取0.5 L 0.2 mol•L-1氯化铁溶液,所得溶液含有0.1 NA个Fe3+ |
13.化学与生产、生活密切相关.下列叙述不正确的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 葡萄糖注射液不能产生丁达尔效应,不属于胶体 | |
| C. | 蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生无关 |
11.如表是元素周期表的一部分,针对表中①~⑩种元素,填写下列空白:
(1)被选作相对原子质量标准的核素是12C(填核素符号).
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物是两性氧化物的元素在第ⅢA族;写出它的氧化物与氢氧化钠溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)从⑤到⑧的元素中,Na原子半径最大(填元素符号).
(5)元素④与⑥形成的化合物属于离子(填“共价”或“离子”)化合物.
(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是C.
A、将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B、比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C、将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D、将⑤、⑥的单质分别在O 2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物是两性氧化物的元素在第ⅢA族;写出它的氧化物与氢氧化钠溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)从⑤到⑧的元素中,Na原子半径最大(填元素符号).
(5)元素④与⑥形成的化合物属于离子(填“共价”或“离子”)化合物.
(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是C.
A、将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B、比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C、将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D、将⑤、⑥的单质分别在O 2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强.
10.下列分子的电子式书写正确的是( )
| A. | 氨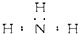 | |
| B. | 四氯化碳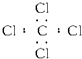 | |
| C. | 氮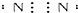 | |
| D. | 二氧化碳${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$C${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$ |
9.现代炼锌的方法可分为火法和湿法两大类.火法炼锌是将闪锌矿(主要含ZnS)焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1100℃~1300℃,使锌蒸馏出来(设空气中N2、O2的体积分数分别为0.80、0.20),主要反应为:
焙烧炉中:2ZnS(s)+3O2(g)→2ZnO(s)+2SO2(g) ①
鼓风炉中:2C(s)+O2(g)→2CO ②
鼓风炉中:ZnO(s)+CO(g)?Zn(g)+CO2(g) ③
(1)已知闪锌矿中含硫的质量分数为16.0%,而所含杂质不含硫,则闪锌矿中硫化锌的质量分数为48.5%.现代工业生产多采用联合生产,可将闪锌矿中的硫用于生产硫酸.现有
此闪锌矿100t,在理论上可生产出98.0%的硫酸50t.
(2)焙烧炉产生的炉气中SO2的体积分数不超过14.3%(保留小数点后一位小数,下同).
(3)鼓风炉容积固定,炉内部分气态物质其物质的量浓度(mol/L)变化如下:
则鼓风炉中CO总的转化率为90.9%;若生产中CO总的利用率为95.0%,列式计算每生产1molZn,至少需要补充焦炭多少克?
(4)若ZnS全部转化为Zn,焙烧炉出来的N2、O2、SO2混合气体中N2占82.5%,鼓风炉中CO的转化率为62.5%,而O2无剩余,试列式计算每生产1mol Zn,应向焙烧炉和鼓风炉中鼓入新鲜空气共多少升(S.T.P)?
焙烧炉中:2ZnS(s)+3O2(g)→2ZnO(s)+2SO2(g) ①
鼓风炉中:2C(s)+O2(g)→2CO ②
鼓风炉中:ZnO(s)+CO(g)?Zn(g)+CO2(g) ③
(1)已知闪锌矿中含硫的质量分数为16.0%,而所含杂质不含硫,则闪锌矿中硫化锌的质量分数为48.5%.现代工业生产多采用联合生产,可将闪锌矿中的硫用于生产硫酸.现有
此闪锌矿100t,在理论上可生产出98.0%的硫酸50t.
(2)焙烧炉产生的炉气中SO2的体积分数不超过14.3%(保留小数点后一位小数,下同).
(3)鼓风炉容积固定,炉内部分气态物质其物质的量浓度(mol/L)变化如下:
| 时间/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.10 | 0.01 | 0.01 |
| 3 | 0.01 | 0.10 | 0.10 |
| 4 | 0.01 | 0.10 | 0.10 |
(4)若ZnS全部转化为Zn,焙烧炉出来的N2、O2、SO2混合气体中N2占82.5%,鼓风炉中CO的转化率为62.5%,而O2无剩余,试列式计算每生产1mol Zn,应向焙烧炉和鼓风炉中鼓入新鲜空气共多少升(S.T.P)?
8.下列实验装置,试剂选用或操作正确的是( )
| A. | 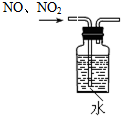 除去NO中的NO2 | B. | 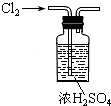 干燥Cl2 | C. | 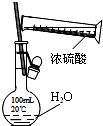 稀释浓硫酸 | D. |  制备少量O2 |
7.某溶液由Na+、Ag+、Ba2+、Al3+、AlO2-、Fe2+、NO3-、Cl-、SO42-中若干种组成,现将溶液分成两等份,再分别通入足量的NH3和SO2充分反应后,最终均有白色沉淀生成.则溶液中一定含有的离子有( )
0 155195 155203 155209 155213 155219 155221 155225 155231 155233 155239 155245 155249 155251 155255 155261 155263 155269 155273 155275 155279 155281 155285 155287 155289 155290 155291 155293 155294 155295 155297 155299 155303 155305 155309 155311 155315 155321 155323 155329 155333 155335 155339 155345 155351 155353 155359 155363 155365 155371 155375 155381 155389 203614
| A. | Al3+、NO3- | B. | Ba2+、Al3+、Cl- | C. | Ba2+、Al3+、NO3- | D. | Ag+、Al3+、NO3- |
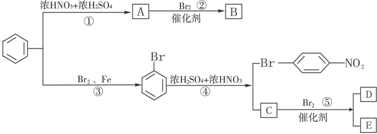
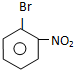 .
. ,E为
,E为 .
. .
.