14.下列物质的类别与所含官能团都正确的是( )
| A. | 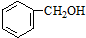 酚类-OH 酚类-OH | B. | 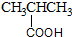 羧酸-COOH 羧酸-COOH | C. |  醛类-CHO 醛类-CHO | D. | CH3OCH3 醚类 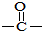 |
11.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- | |
| B. | pH=1的溶液中:Fe2+、NO3-、AlO2-、Na+ | |
| C. | 水电离出的c(H+)=10-12 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO42-、SCN- |
9.有机物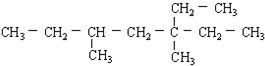 的一氯代物的同分异构体有几种?( )
的一氯代物的同分异构体有几种?( )
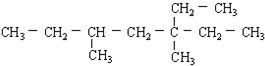 的一氯代物的同分异构体有几种?( )
的一氯代物的同分异构体有几种?( )| A. | 7 | B. | 8 | C. | 9 | D. | 10 |
8.动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制H2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等.
仪器:①烧杯,②试管,③酒精灯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
①Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2+H2↑,②H2S+Cl2═2HCl+S↓,此实验的结论:同一周期元素从左到右,金属性减弱,非金属性增强.
(4)请你补充一组实验方案(简单易行),证明此周期中另两种主族元素的性质递变规律.向硅酸钠溶液中加入磷酸溶液,有白色沉淀生成,说明磷酸的酸性比硅酸强,即非金属性:P>Si.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的H2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制H2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等.
仪器:①烧杯,②试管,③酒精灯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
(4)请你补充一组实验方案(简单易行),证明此周期中另两种主族元素的性质递变规律.向硅酸钠溶液中加入磷酸溶液,有白色沉淀生成,说明磷酸的酸性比硅酸强,即非金属性:P>Si.
7.元素周期表是学习化学的重要工具,它隐含着周期表中所反映的许多信息和规律.下表所列是五种短周期的原子半径及主要化合价
(1)用元素代号标出它们在周期表中对应位置(以下为周期表的一部分).
(2)B元素处于周期表中三周期ⅢA族;
(3)在元素周期表中金属与非金属的分界处,可以找到制半导体材料的元素;
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(5)用电子式表示A、D形成化合物的过程 ;
;
(6)C、E形成化合物为SO2、SO3(填化学式).
0 155183 155191 155197 155201 155207 155209 155213 155219 155221 155227 155233 155237 155239 155243 155249 155251 155257 155261 155263 155267 155269 155273 155275 155277 155278 155279 155281 155282 155283 155285 155287 155291 155293 155297 155299 155303 155309 155311 155317 155321 155323 155327 155333 155339 155341 155347 155351 155353 155359 155363 155369 155377 203614
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(3)在元素周期表中金属与非金属的分界处,可以找到制半导体材料的元素;
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(5)用电子式表示A、D形成化合物的过程
 ;
;(6)C、E形成化合物为SO2、SO3(填化学式).
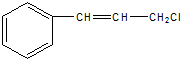 中官能团的名称:碳碳双键、氯原子.
中官能团的名称:碳碳双键、氯原子.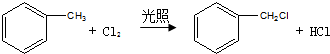 .
.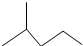 所表示物质的名称是:2-甲基戊烷.
所表示物质的名称是:2-甲基戊烷.