15.乙醛(CH3CHO)、乙酸、乙酸乙酯三种有机物按一定比例组成的混合物中,若含氧的质量分数为A%,则此混合物中含氢的质量分数为( )
| A. | $\frac{6A%}{7}$ | B. | $\frac{1-A%}{7}$ | C. | $\frac{6(1-A%)}{7}$ | D. | (100-$\frac{7A}{6}$)% |
14.某炔烃与氢气加成后得到2,2-二甲基丁烷,该炔烃的名称是( )
| A. | 3,3-二甲基-1-丁烯 | B. | 2,2-二甲基-2-丁烯 | ||
| C. | 2,2-二甲基-3-丁炔 | D. | 3,3-二甲基-1-丁炔 |
13.下列叙述错误的是( )
| A. | ⅡA族元素的阳离子与上周期稀有气体元素的原子具有相同的核外电子排布 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 多电子原子中,在离核较近的区域内运动的电子能量较低 | |
| D. | 两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键 |
12.有短周期元素X、Y、Z、D、E,其中X、Y、Z、D在周期表中的相对位置如下表,已知X与Y的原子序数之和等于Z的核电荷数,E与Z为同周期元素,0.2mol E与足量盐酸反应,得到2.24L气体(标准状况).回答下列问题:
(1)写出元素名称:X氮,E钠.
(2)X、D的氢化物相遇时产生的现象是冒白烟.
(3)X的最高价氧化物的水化物M,其稀溶液能与Z的低价氧化物反应,离子方程式为2NO3-+3SO2+2H2O═4H++2NO↑+3SO42-,则M的稀溶液的氧化性大于Z的最高价氧化物的水化物的稀溶液的氧化性(填“大于”、“等于”或“小于”).
(4)E的某种氧化物能与水发生氧化还原反应,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.0.1mol E的该氧化物完全反应,转移电子数目为0.1NA.
| X | Y | |
| Z | D |
(2)X、D的氢化物相遇时产生的现象是冒白烟.
(3)X的最高价氧化物的水化物M,其稀溶液能与Z的低价氧化物反应,离子方程式为2NO3-+3SO2+2H2O═4H++2NO↑+3SO42-,则M的稀溶液的氧化性大于Z的最高价氧化物的水化物的稀溶液的氧化性(填“大于”、“等于”或“小于”).
(4)E的某种氧化物能与水发生氧化还原反应,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.0.1mol E的该氧化物完全反应,转移电子数目为0.1NA.
11.下列物质中,既含有离子键又含有非极性共价键的是( )
| A. | H2S | B. | CO2 | C. | K2O2 | D. | Na2CO3 |
10.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下反应 |
| B | 将可调高度的铜丝伸入到HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| C | 将浓硫酸滴到蔗糖表面 | 固体变黑 | 浓硫酸具有脱水性和强酸性 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
9.已知元素的某种性质“x”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的x的数值:
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的x差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键.
(2)根据上表给出的数据,简述主族元素的x的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强).
(3)简述第二周期元素(除稀有气体外)的x的数值大小与原子半径之间的关系:原子半径越小,X的数值越大.
(4)请你预测Br与I元素的x数值的大小关系:Br>I(填“>”、“=”或“<”).
(5)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
| 元素 | Al | B | Be | C | Cl | F | Li |
| x的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| x的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
(1)经验规律告诉我们:当形成化学键的两原子相应元素的x差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键.
(2)根据上表给出的数据,简述主族元素的x的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强).
(3)简述第二周期元素(除稀有气体外)的x的数值大小与原子半径之间的关系:原子半径越小,X的数值越大.
(4)请你预测Br与I元素的x数值的大小关系:Br>I(填“>”、“=”或“<”).
(5)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
8.下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.
(1)上述元素的单质中熔点最高的可能是石墨(填名称).
(2)D的氢化物比G的氢化物稳定,其原因是D的非金属性比G的强的缘故.
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”),用电子式表示该物质的形成过程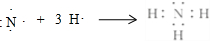 .
.
(4)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的C、F(填字母序号)元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2=2Na2CO3+O2
(5)飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为N2,其电子式为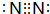 .
.
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
(2)D的氢化物比G的氢化物稳定,其原因是D的非金属性比G的强的缘故.
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”),用电子式表示该物质的形成过程
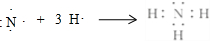 .
.(4)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的C、F(填字母序号)元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2=2Na2CO3+O2
(5)飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为N2,其电子式为
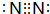 .
.
7.用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
| A. | 1g H2含有的氢原子数目为NA | |
| B. | 常温常压下,22.4L O2含有的分子数目为NA | |
| C. | 1L1mol•L-1KOH溶液中含有的钾离子数目为NA | |
| D. | 1molZn变为Zn2+失去的电子数目为NA |
6.a.b.c.d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c.下列叙述错误的是( )
0 155177 155185 155191 155195 155201 155203 155207 155213 155215 155221 155227 155231 155233 155237 155243 155245 155251 155255 155257 155261 155263 155267 155269 155271 155272 155273 155275 155276 155277 155279 155281 155285 155287 155291 155293 155297 155303 155305 155311 155315 155317 155321 155327 155333 155335 155341 155345 155347 155353 155357 155363 155371 203614
| A. | d元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | 只有a与其他元素生成的化合物都是离子化合物 | |
| D. | a.b.c.d与氢形成的化合物中化学键均为极性共价键 |