6.Li-Al/FeS电池是一种正在开发的车载锂电池,该电池中正极的电极反应式为:2Li++FeS+2e-═Li2S+Fe有关该电池的下列说法中,正确的是( )
| A. | 该电池的电池反应式为:2Li+FeS═Li2S+Fe | |
| B. | Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价 | |
| C. | 负极的电极反应式为Al-3e-═Al3+ | |
| D. | 电解质溶液可以是氢氧化钠溶液或者稀硫酸 |
5.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备手机电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| B. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| C. | 元素X与氢形成的化合物可能既有极性键又有非极性键 | |
| D. | 元素Z可与元素X形成共价化合物XZ2 |
4.如表实验不能达到预期实验目的是( )
| 序号 | 实验操作 | 实验目的 |
| A | 在浓硫酸和稀硫酸中分别加入Cu片,加热 | 比较稀、浓硫酸氧化性强弱 |
| B | F2、Cl2分别与H2反应 | 比较氟、氯的非金属性强弱 |
| C | 把CO2通入到水玻璃中 | 比较碳、硅的非金属性强弱 |
| D | 向MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
3.下列各组金属和液体(配有导线),能组成原电池的是( )
| A. | Cu、Cu、稀硫酸 | B. | C、Pt、氯化钠溶液 | C. | Cu、Zn、酒精 | D. | Fe、Cu、FeCl3溶液 |
2.把a、b、c、d 四块金属片浸人稀酸中,用导线两两相连组成原电池.若a、b相连时,a为负极;c、d相连时,电子由c到d;a、c相连时c极上产生大量气泡;b、d相连时,d为负极.则四种金属的活动性顺序由强到弱的顺序为( )
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
1.元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为( )
| A. | XY2 | B. | X2Y3 | C. | X3Y2 | D. | XY |
20.实验室用锌与稀硫酸制取氢气,欲提高反应速率可采取的措施是( )
0 155170 155178 155184 155188 155194 155196 155200 155206 155208 155214 155220 155224 155226 155230 155236 155238 155244 155248 155250 155254 155256 155260 155262 155264 155265 155266 155268 155269 155270 155272 155274 155278 155280 155284 155286 155290 155296 155298 155304 155308 155310 155314 155320 155326 155328 155334 155338 155340 155346 155350 155356 155364 203614
| A. | 将稀硫酸改成浓硫酸 | B. | 将纯锌换成含铜、铅等杂质的粗锌 | ||
| C. | 往稀硫酸中滴加浓度更大的硝酸 | D. | 往稀硫酸中加入K2SO4溶液 |
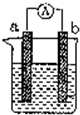 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: