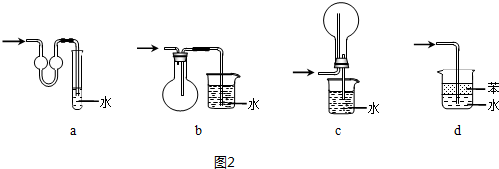
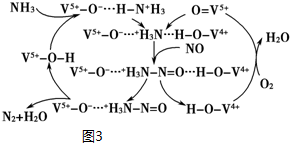
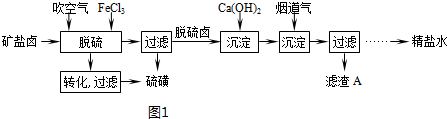
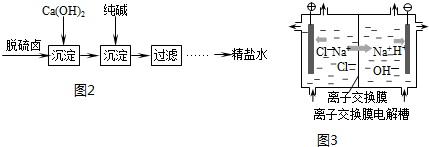
9.X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素.X和R属同族元素;Z和U位于第VII A族;X和Z可形成化合物XZ4;Q原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃.
完成下列填空:
(1)R原子的电子排布式是1s22s22p63s23p2;X所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3;Z的氢化物的水溶液可用于雕刻玻璃;Q、R、U的单质形成的晶体,熔点由高到低的排列顺序是Si>Mg>Cl2.
(2)CuSO4能用作T4中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的化学方程式是10CuSO4+P4+16H2O→4H3PO4+10Cu+10H2SO4.
在pH为4~5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀.工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右,再慢慢加入粗氧化铜(含FeO),充分搅拌使之溶解.
(3)除去该溶液中杂质离子的方法是在溶液中通入Cl2,再加入CuO粉末调节pH为4~5.
碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
(4)硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是硅烷中的Si-Si键和Si-H键的键能小于烷烃分子中C-C键和C-H键的键能,稳定性差,易断裂,导致长链硅烷难以形成.
第三周期部分元素氟化物的熔点如下:
(5)表中三种氟化物熔点差异的原因是NaF与MgF2为离子晶体,而SiF4为分子晶体,所以NaF与MgF2远比SiF4熔点要高;又因为Mg2+的半径小于Na+的半径,所以MgF2中离子键的强度大于NaF中离子键的强度,故MgF2的熔点高于NaF.
完成下列填空:
(1)R原子的电子排布式是1s22s22p63s23p2;X所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3;Z的氢化物的水溶液可用于雕刻玻璃;Q、R、U的单质形成的晶体,熔点由高到低的排列顺序是Si>Mg>Cl2.
(2)CuSO4能用作T4中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的化学方程式是10CuSO4+P4+16H2O→4H3PO4+10Cu+10H2SO4.
在pH为4~5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀.工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右,再慢慢加入粗氧化铜(含FeO),充分搅拌使之溶解.
(3)除去该溶液中杂质离子的方法是在溶液中通入Cl2,再加入CuO粉末调节pH为4~5.
碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | Si-Si | Si-H |
| 键能(KJ/mol) | 356 | 413 | 226 | 318 |
第三周期部分元素氟化物的熔点如下:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
8.硝酸与金属反应时,浓度越稀还原产物价态越低.现用一定量的铝粉与镁粉组成的混合物与100mL硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,向反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与产生的沉淀质量的关系如图所示.下列结论正确的是( )
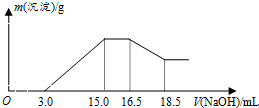

| A. | 铝与混合溶液反应的离子方程式为8Al+30H++3NO3-→8Al3++3NH4++9H2O | |
| B. | 参加反应硝酸根离子物质的量为0.06mol | |
| C. | 参加反应的铝与镁的质量之比为4:3 | |
| D. | 混合液中硫酸的物质的量的浓度为0.36mol/L |
7.已知某溶液中含有碳酸钠、硫酸钠、氢氧化钠、氯化钠四种溶质,欲将该溶液中四种溶质的阴离子逐一检验出来,所加试剂先后顺序合理的是( )
| A. | HNO3、Ba(NO3)2、NH4NO3、AgNO3 | B. | HNO3、NH4NO3、Ba(NO3)2、AgNO3 | ||
| C. | NH4NO3、HNO3、Ba(NO3)2、AgNO3 | D. | NH4NO3、HNO3、AgNO3、Ba(NO3)2 |
5.摩尔盐在工业上有重要的用途.已知其由一种阴离子,两种阳离子组成的晶体,某学习小组按如下实验测定摩尔盐样品的组成.步骤如下:
①称取3.920g摩尔盐样品配制250mL溶液.
②取少量配制溶液,加入KSCN溶液,无明显现象.
③另取少量配制溶液,加入过量浓氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体和红褐色沉淀.
④定量测定如下:
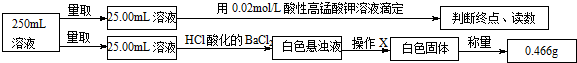
滴定实验结果记录如下:
完成下列填空:
(1)步骤①中需要的定量仪器为电子天平、250mL容量瓶.
(2)步骤②的目的是确定红褐色沉淀中的铁元素在摩尔盐中是以亚铁离子形式存在.产生红褐色沉淀的离子方程式4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓.
(3)步骤④中操作X为过滤、洗涤、干燥或烘干(冷却)(按操作顺序填写).
(4)步骤④中酸性高锰酸钾溶液能否用碘的酒精溶液代替,不能(填“能”或“不能”),请说明理由碘单质与亚铁离子不反应.
(5)步骤④若在滴定过程中,待测液久置,消耗高锰酸钾溶液的体积将偏小.(选填“偏大”、“偏小”或“不变”).
(6)通过上述实验测定结果,推断摩尔盐化学式为(NH4)2SO4•FeSO4•6H2O或(NH4)2Fe(SO4)2•6H2O.
①称取3.920g摩尔盐样品配制250mL溶液.
②取少量配制溶液,加入KSCN溶液,无明显现象.
③另取少量配制溶液,加入过量浓氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体和红褐色沉淀.
④定量测定如下:

滴定实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
(1)步骤①中需要的定量仪器为电子天平、250mL容量瓶.
(2)步骤②的目的是确定红褐色沉淀中的铁元素在摩尔盐中是以亚铁离子形式存在.产生红褐色沉淀的离子方程式4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓.
(3)步骤④中操作X为过滤、洗涤、干燥或烘干(冷却)(按操作顺序填写).
(4)步骤④中酸性高锰酸钾溶液能否用碘的酒精溶液代替,不能(填“能”或“不能”),请说明理由碘单质与亚铁离子不反应.
(5)步骤④若在滴定过程中,待测液久置,消耗高锰酸钾溶液的体积将偏小.(选填“偏大”、“偏小”或“不变”).
(6)通过上述实验测定结果,推断摩尔盐化学式为(NH4)2SO4•FeSO4•6H2O或(NH4)2Fe(SO4)2•6H2O.
3.向100mLNa2CO3与NaAlO2的混合溶液中逐滴加入1mol/L的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.下列说法正确的是( )
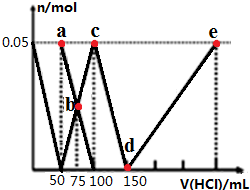

| A. | 原混合溶液中的n(CO32-):n(AlO2-)=1:1 | |
| B. | a点溶液中:c(HCO3-)+c(H2CO3)+c(H+)=c(OH-) | |
| C. | b点溶液中浓度顺序为:c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-) | |
| D. | d→e的过程中水的电离程度逐渐减小 |
2.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.说法正确的是( )
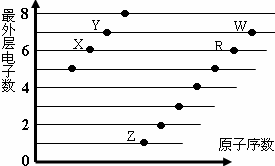

| A. | 元素非金属性:X>R>W | |
| B. | X与R形成的分子内含两种作用力 | |
| C. | X、Z形成的化合物中可能含有共价键 | |
| D. | 元素对应的离子半径:W>R>X |
1.下列卤代烃不能够由烃经加成反应制得的是( )
0 155162 155170 155176 155180 155186 155188 155192 155198 155200 155206 155212 155216 155218 155222 155228 155230 155236 155240 155242 155246 155248 155252 155254 155256 155257 155258 155260 155261 155262 155264 155266 155270 155272 155276 155278 155282 155288 155290 155296 155300 155302 155306 155312 155318 155320 155326 155330 155332 155338 155342 155348 155356 203614
| A. | 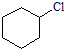 | B. | 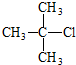 | C. | 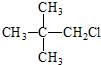 | D. | 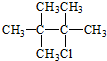 |
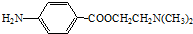 )可用作临床麻醉剂,熔点约60℃.它的一条合成路线如下图所示(部分反应试剂和条件已省略):
)可用作临床麻醉剂,熔点约60℃.它的一条合成路线如下图所示(部分反应试剂和条件已省略):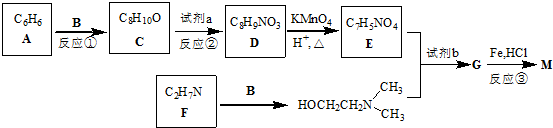
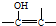 的结构不稳定.
的结构不稳定.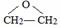 FH3C-NH-CH3
FH3C-NH-CH3 .
.