2.莫尔盐,简称FAS,蓝绿色的无机复盐,在空气中逐渐风化及氧化,其名来源于德国化学家莫尔(Karl Friedrich Mohr).工业常用的制备方法是从废铁屑中回收铁屑(不含铁之外的其他金属元素),经碱溶液洗净之后,用过量硫酸溶解;再加入稍过量硫酸铵饱和溶液,在小火下蒸发溶剂直到晶膜出现,停火利用余热蒸发溶剂;过滤后用少量乙醇洗涤.莫尔盐的化学式可能是( )
| A. | NH4Fe(SO4)2•12H2O | B. | NH4Al(SO4)2•12H2O | C. | (NH4)2Fe(SO4)2•6H2O | D. | (NH4)2Fe(SO4)2 |
1.下列电子式书写正确的是( )
| A. | 硫化钠的形成过程: | B. | CCl4: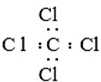 | ||
| C. | 氮气:N:N: | D. | 二氧化碳: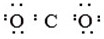 |
20.NA表示阿伏加德罗常数.下列叙述正确的是( )
| A. | 通常状况下,1mol/L Na2CO3溶液中含钠离子数为2NA | |
| B. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| C. | 1mol N5+含有的电子数为34NA | |
| D. | 1mol NH4+中含有的中子数为10NA |
19.在人类已知的化合物中,品种最多的是( )
| A. | 元素周期表里属于过渡元素的化合物 | |
| B. | 位于元素周期表里第ⅡA族元素的化合物 | |
| C. | 位于元素周期表里第ⅢA族元素的化合物 | |
| D. | 位于元素周期表里第ⅣA族元素的化合物 |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 34g质量分数为4%的H2O2水溶液中含氧原子数目为0.08NA | |
| B. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92kJ/mol,若放出热量4.6kJ,则转移电子数目为0.3NA | |
| C. | 0.1mol•L-1Na2S溶液中所含S2-总数小于0.1NA | |
| D. | 6.4gCu与40mL10mol•L-1浓硝酸作用能生成NO2的分子数为0.2NA |
16. 某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )
某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )
 某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )
某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )| A. | 分子式为C12H18O2 | |
| B. | 能发生加成反应、取代反应和消去反应 | |
| C. | 能使酸性KMn04溶液和溴水褪色,且褪色原理相同 | |
| D. | 1mol该有机物在一定条件下和H2反应,共消耗H2为2mol |
15.在一定条件下,反应2A(g)+B(g)?2C(g)在一密闭容器中达到平衡.充入适量B气体并维持B浓度和容器的温度不变,增大容器的体积,跟原平衡相比较达到新平衡时A的转化率将( )
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 无法判断 |
14.室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A. | 加水稀释2倍后,两溶液的pH均减小 | |
| B. | 使温度都升高20℃后,两溶液的pH均不变 | |
| C. | 加适量的醋酸钠晶体后,盐酸pH增大,醋酸pH不变 | |
| D. | 加足量的锌充分反应后,醋酸产生的氢气比盐酸多 |
13.下列实验操作能达到目的是( )
0 155152 155160 155166 155170 155176 155178 155182 155188 155190 155196 155202 155206 155208 155212 155218 155220 155226 155230 155232 155236 155238 155242 155244 155246 155247 155248 155250 155251 155252 155254 155256 155260 155262 155266 155268 155272 155278 155280 155286 155290 155292 155296 155302 155308 155310 155316 155320 155322 155328 155332 155338 155346 203614
| A. | 加热氯化铵固体制取氨气 | |
| B. | 检验乙醇中是否含水:用无水硫酸铜,观察是否变蓝色 | |
| C. | 除去乙醛中的乙酸杂质:加入氢氧化钠溶液洗涤,分液 | |
| D. | 滴有酚酞的碳酸钠中,加入氯化钡溶液后,红色变浅,证明碳酸钠溶液中存在水解平衡 |
 ),写出有关方程式,并注明反应类型.
),写出有关方程式,并注明反应类型.