20.离子方程式Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O可表示( )
| A. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比2:1反应 | |
| B. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比1:2反应 | |
| C. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比2:1反应 | |
| D. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比1:2反应 |
19.Cl2可用于废水处理.向KCN溶液中先加入足量KOH溶液再通入氯气,充分反应后生成两种无毒的气体.下列说法正确的是( )
| A. | 两种无毒的气体均为还原产物 | |
| B. | 反应后溶液的pH会升高 | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 每转移2NA个电子时,一定会生成13.44 L的气体 |
18.下列实验说法正确的是( )
| A. | 将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3 | |
| B. | 2mL10%的NaOH溶液中滴加2%的CuSO4溶液4~6滴制得新制氢氧化铜 | |
| C. | 将水蒸气通过灼热的铁粉,铁粉变红棕色,说明铁与水在高温下能发生反应 | |
| D. | 取a克Na2CO3和NaHCO3混合物与少量稀盐酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体,可测得Na2CO3质量分数 |
17.关于反应2HI(g)?H2(g)+I2(g)-11kJ,正确的是( )
| A. | 反应物的总键能低于生成物的总键能 | |
| B. | 1mol I2(g)中通入1mol H2(g),反应放热11kJ | |
| C. | 等物质的量时,I2(g)具有的能量低于I2(l) | |
| D. | 平衡时分离出HI(g),正反应速率先减小后增大 |
16.钢铁防护方法有多种,如图中的方法描述正确的是( )


| A. | b为电源负极 | |
| B. | 该方法是牺牲阳极的阴极保护法 | |
| C. | 电子流向:a→钢铁闸门→辅助电极→b→a | |
| D. | 电源改用导线连接进行防护时,辅助电极发生氧化反应 |
15.某有机化合物的结构简式如图所示,下列说法正确的是( )


| A. | 不能发生银镜发应 | |
| B. | 1mol 该物质最多可与2molBr2反应 | |
| C. | 1mol 该物质最多可与4mol NaOH反应 | |
| D. | 与NaHCO3、Na2CO3均能发生反应 |
14.能使氢硫酸溶液的pH先升高后降低的物质是( )
| A. | Cl2 | B. | SO2 | C. | CuSO4 | D. | O2 |
13.工业生产措施中,能同时提高反应速率和产率的是( )
0 155144 155152 155158 155162 155168 155170 155174 155180 155182 155188 155194 155198 155200 155204 155210 155212 155218 155222 155224 155228 155230 155234 155236 155238 155239 155240 155242 155243 155244 155246 155248 155252 155254 155258 155260 155264 155270 155272 155278 155282 155284 155288 155294 155300 155302 155308 155312 155314 155320 155324 155330 155338 203614
| A. | 合成氨使用高压 | B. | 制硝酸用Pt-Rh合金作催化剂 | ||
| C. | 制硫酸时接触室使用较高温度 | D. | 侯氏制碱法循环利用母液 |
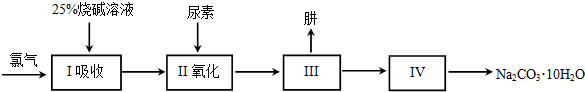
 .
.