2.正确使用化学用语是学好化学的基础,下列化学用语正确的是( )
| A. | 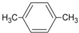 的名称:1,4-二甲苯 的名称:1,4-二甲苯 | B. | 丙烷的分子式:CH3CH2CH3 | ||
| C. | 聚丙烯的链节:-CH2-CH2-CH2- | D. | H2S的电子式: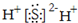 |
1.人类已经成功合成了117号元素Uus,关于${\;}_{117}^{294}$Uus的叙述正确的是( )
| A. | 原子内电子数多于中子数 | B. | 与${\;}_{117}^{296}$Uus电子式相同 | ||
| C. | 元素的近似相对原子质量是294 | D. | 处于不完全周期内 |
20.下列有关溶液中离子存在和转化的表达合理的是( )
| A. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- | |
| B. | 标准状况下,将1.12 L CO2气体通入1 L 0.1 mol/L的NaAlO2溶液中:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 由水电离出的c(H+)=1×10-12 mol/L 的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| D. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓ |
19.为了保护环境,充分利用资源.某研究小组通过如图简化流程,将工业制硫酸的硫铁矿烧渣(主要以Fe2O3存在,还含有氧化铝、二氧化硅等杂质)转变成重要的化工原料FeSO4(反应条件略)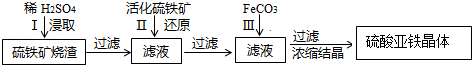
活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(S04)3+8H2O→15FeSO4+8H2SO4,不考虑其它反应,已知各氢氧化物沉淀PH值,请回答下列问题:
(1)第Ⅲ步目的是调剂PH,去除铝杂质(或除去Al(OH)3\Fe(OH)3).
(2)检验所得绿矾晶体中是否含有Fe3+的实验操作为取少量晶体溶于水,滴加KSCN溶液,若不出现血红色,(或滴加苯酚溶液,不出现紫色)表明不含有Fe3+,反之则含.
(3)得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质,②温度低、用水少降低洗涤过程中硫酸亚铁晶体的损耗.
研究性学习小组对硫酸亚铁晶体(FeSO4•xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究:
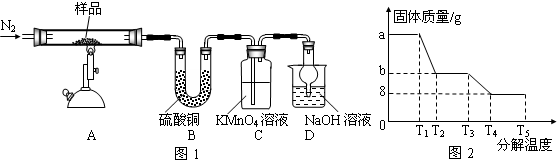
(4)装置B的目的是检验产物水生成;装置C中高锰酸钾溶液褪色,使之褪色的物质的名称是二氧化硫;装置D中球形干燥管的作用是防止氢氧化钠溶液倒吸.
(5)硫酸亚铁晶体完全分解后装置A中残留红棕色固体.写出FeSO4分解的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(6)设计一个简单实验检验产生的含硫元素的气体: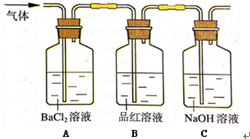 .
.
(7)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量--分解温度的关系如图2,由此得出FeSO4•xH2O中的x值为$\frac{10a-152}{18}$.

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(S04)3+8H2O→15FeSO4+8H2SO4,不考虑其它反应,已知各氢氧化物沉淀PH值,请回答下列问题:
| pH | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 5.8 | 8.8 |
| Fe(OH)3 | 1.1 | 3.2 |
| Al(OH)3 | 3.0 | 5.0 |
(2)检验所得绿矾晶体中是否含有Fe3+的实验操作为取少量晶体溶于水,滴加KSCN溶液,若不出现血红色,(或滴加苯酚溶液,不出现紫色)表明不含有Fe3+,反之则含.
(3)得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质,②温度低、用水少降低洗涤过程中硫酸亚铁晶体的损耗.
研究性学习小组对硫酸亚铁晶体(FeSO4•xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究:

(4)装置B的目的是检验产物水生成;装置C中高锰酸钾溶液褪色,使之褪色的物质的名称是二氧化硫;装置D中球形干燥管的作用是防止氢氧化钠溶液倒吸.
(5)硫酸亚铁晶体完全分解后装置A中残留红棕色固体.写出FeSO4分解的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(6)设计一个简单实验检验产生的含硫元素的气体:
 .
.(7)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量--分解温度的关系如图2,由此得出FeSO4•xH2O中的x值为$\frac{10a-152}{18}$.
18.在含有2mol复盐NH4Al(SO4)2的溶液中加入Ba(OH)2溶液,若生成4mol沉淀,则加入的Ba(OH)2的物质的量可能为( )
| A. | 6mol | B. | 4.7mol | C. | 3mol | D. | 2.4mol |
17.常温下用 a L pH=3的HX溶液与 b L pH=11的氢氧化钠溶液相混合,下列叙述正确的是( )
| A. | 若二者恰好中和,则一定是 a=b | B. | 若混合液显碱性,则一定是 b≥a | ||
| C. | 若混合液显中性,则一定是 a≤b | D. | 若混合液显酸性,则一定是 a>b |
16.下列实验操作或结论正确的是( )
| A. | 为测定新制氯水的pH值,用玻璃棒蘸取待测液滴在pH试纸上,与比色卡对照即可 | |
| B. | 做蒸馏实验时,如果在液体沸腾前发现忘记加沸石,应立即停止加热,冷却后补加沸石 | |
| C. | 在未知液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知液中存在SO32-、SO42- | |
| D. | 提纯混有少量硝酸钾的氯化钠,采用在较高的温度下制成浓溶液再冷却结晶、过滤、干燥的方法 |
15.向300mlKOH溶液中缓慢通入2.24L(标准状况下)CO2气体,CO2完全反应后,再小心减压蒸干溶液,得到11.9g白色固体.则下列说法中正确的是( )
| A. | 二氧化碳通入溶液后,先生成KHCO3 | |
| B. | 此白色固体可能为KOH 和K2CO3 | |
| C. | 原KOH溶液中物质的量浓度一定是0.500mol/L | |
| D. | 此白色固体可能有两种组成情况,这两种混合物都有含有K2CO3 |
13.我国科学家屠呦呦因在抗疟疾药物---青蒿素的开发起到关键作用而获2015年诺贝尔生理学或医学奖.青蒿素可由香草醛经过系列反应合成,下列是主要原料、中间体、产品:
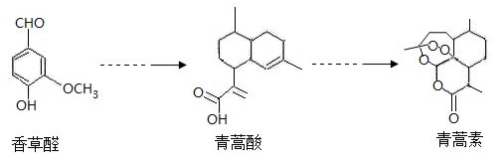
下列有关说法中错误的是( )
0 155140 155148 155154 155158 155164 155166 155170 155176 155178 155184 155190 155194 155196 155200 155206 155208 155214 155218 155220 155224 155226 155230 155232 155234 155235 155236 155238 155239 155240 155242 155244 155248 155250 155254 155256 155260 155266 155268 155274 155278 155280 155284 155290 155296 155298 155304 155308 155310 155316 155320 155326 155334 203614

下列有关说法中错误的是( )
| A. | 青蒿素能发生水解反应 | |
| B. | 青蒿素易溶于乙醚 | |
| C. | 在一定条件下,香草醛可与HCHO发生缩聚反应 | |
| D. | 可用FeCl3 溶液或 NaHCO3溶液鉴别香草醛和青蒿酸 |