17.下列物质属于纯净物的是( )
| A. | 漂粉精 | B. | 铝热剂 | C. | 汽油 | D. | 纯碱 |
14.已知aRO4x-+bH++cCl-═dR2++5Cl2↑+8H2O,则RO4x-中R的化合价为( )
| A. | +4 | B. | +5 | C. | +6 | D. | +7 |
10.进行钠与水反应的实验,实验现象归纳表中.为了解释这些现象,请从“供选择的理由”栏中,选择适合的字母代号填入对应的空格中.
| 序号 | 实验现象 | 答案 | 供选择的理由 |
| (1) | 小刀能切割钠块 | C | A有碱(NaOH)生成 B钠密度小于水的密度,钠球表面生成气体(H2)速率不同 C钠硬度较小 D钠的熔点较低,发生放热反应 |
| (2) | 钠溶液化成闪亮的小球 | D | |
| (3) | 钠球浮在水面上,四处游动 | B | |
| (4) | 水中酚酞变红色 | A |
8.如图所示的实验操作,不能达到相应目的是( )
0 155127 155135 155141 155145 155151 155153 155157 155163 155165 155171 155177 155181 155183 155187 155193 155195 155201 155205 155207 155211 155213 155217 155219 155221 155222 155223 155225 155226 155227 155229 155231 155235 155237 155241 155243 155247 155253 155255 155261 155265 155267 155271 155277 155283 155285 155291 155295 155297 155303 155307 155313 155321 203614
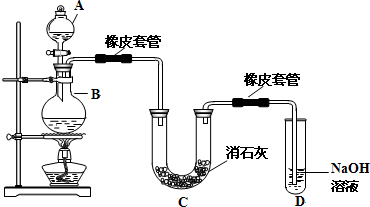
| A. | 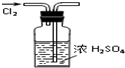 干燥Cl2 | B. | 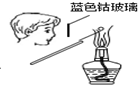 检验K2CO3中的K+ | C. | 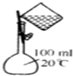 转移溶液 | D. | 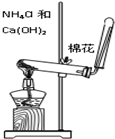 实验室制氨气 |