14.氢气是人类最理想的能源.已知在25℃、101 kPa下,1 g氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
| A. | 2H2+O2═2H2O△H=-571.6 kJ/mol | B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g )△H=-285.8kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | D. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ/mol |
13.如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )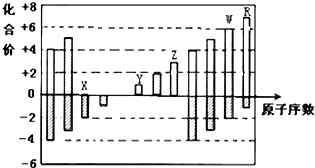

| A. | 原子半径:Z>Y>X | |
| B. | 气态氢化物的稳定性:R<W | |
| C. | Y和Z两者最高价氧化物对应的水化物能相互反应 | |
| D. | WX3和水反应形成的化合物是离子化合物 |
12.有A、B、C、D、E五种金属元素.在相同条件下,B元素的最高价氧化物对应水化物的碱性比A的弱;B、C与硫酸构成的原电池中B为负极;D单质可以与冷水剧烈反应并放出氢气;A、B、C、E四种单质分别投入盐酸中,只有E不放出氢气.则五种金属元素的金属性由强到弱的顺序为( )
| A. | D>B>A>C>E | B. | D>A>B>C>E | C. | A>B>C>E>D | D. | D>E>B>A>C |
11.CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用分别是( )
| A. | 分子间作用力,离子键 | B. | 化学键,分子间作用力 | ||
| C. | 化学键,化学键 | D. | 分子间作用力,分子间作用力 |
10.用铁片和稀硫酸反应制氢气时,下列措施不能使氢气生成速率加快的是( )
| A. | 不用稀硫酸改用98%的浓硫酸 | B. | 加热 | ||
| C. | 滴加CuSO4溶液 | D. | 不用铁片改用铁粉 |
9.一定条件下,在体积一定的密闭容器中加入1mol N2和3mol H2发生反应:N2+3H2 $?_{催化剂}^{高温高压}$2NH3(正反应是放热反应).下列有关说法正确的是( )
| A. | 达到化学反应限度时,可生成2mol NH3 | |
| B. | 向容器中再加入N2,可以加快反应速率 | |
| C. | 降低温度可以加快反应速率 | |
| D. | 1mol N2 和3mol H2的总能量低于2mol NH3的总能量 |
8.下列各组元素的原子序数中,其相应的元素原子能形成X2Y共价化合物的是( )
0 155119 155127 155133 155137 155143 155145 155149 155155 155157 155163 155169 155173 155175 155179 155185 155187 155193 155197 155199 155203 155205 155209 155211 155213 155214 155215 155217 155218 155219 155221 155223 155227 155229 155233 155235 155239 155245 155247 155253 155257 155259 155263 155269 155275 155277 155283 155287 155289 155295 155299 155305 155313 203614
| A. | 11与16 | B. | 1与8 | C. | 12与17 | D. | 6与8 |
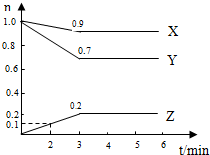 某温度时,在2L容器中X.、Y、Z三种物质的物质的量随时间变化曲线
某温度时,在2L容器中X.、Y、Z三种物质的物质的量随时间变化曲线 ,(2)NH3:
,(2)NH3: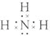 ,
,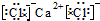 ,(4)CO2:
,(4)CO2: .
.