7.下列反应中,符合如图所示能量变化的是( )
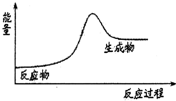

| A. | H2在Cl2中燃烧 | B. | Ba(OH)2•8H2O和NH4Cl固体的反应 | ||
| C. | Na和H2O的反应 | D. | 生石灰溶于水 |
6.下列说法不正确的是( )
| A. | 金刚石和石墨互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | |
| D. | 分子式为C4H10的物质为纯净物 |
5.某元素最高价氧化物对应水化物的化学式是H3XO4,这种元素的气态氢化物的分子式为( )
| A. | HX | B. | XH3 | C. | H2X | D. | XH4 |
4.下列各组物质的晶体中,化学键类型和晶体类型均相同的是( )
| A. | NH3和NH4Cl | B. | HCl和SiO2 | C. | CO2和H2O | D. | KCl和K |
3.下列物质中,既有离子键又有共价键的是( )
| A. | MgCl2 | B. | NH4Cl | C. | CO2 | D. | H2S |
20.下列说法中正确的是( )
0 155118 155126 155132 155136 155142 155144 155148 155154 155156 155162 155168 155172 155174 155178 155184 155186 155192 155196 155198 155202 155204 155208 155210 155212 155213 155214 155216 155217 155218 155220 155222 155226 155228 155232 155234 155238 155244 155246 155252 155256 155258 155262 155268 155274 155276 155282 155286 155288 155294 155298 155304 155312 203614
| A. | 常温下,2A(s)+B(g)=2C(g)+D(g)不能自发进行,则该反应焓变一定大于零 | |
| B. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件下和点燃条件下的△H不同 | |
| C. | 含1mol硫酸的稀溶液与含1molBa(OH)2的稀溶液完全中和所放出的热量为中和热 | |
| D. | 在25℃、101KPa时,2mol 氢气的燃烧热是1mol 氢气的2倍 |
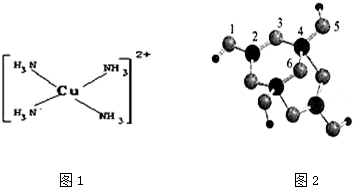
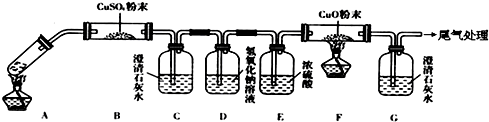
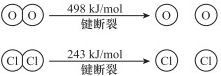
 .
.
