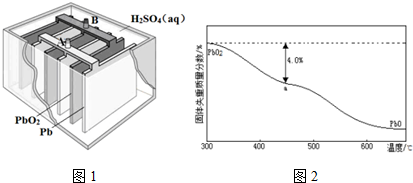
17.某实验小组依据反应AsO43-+2H++2I-?AsO33-+I2+H2O设计如图1原电池,探究pH对AsO43-氧化性的影响.测得电压与pH的关系如图2.下列有关叙述错误的是( )
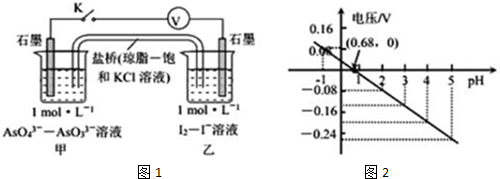

| A. | pH>0.68时,甲烧杯中石墨为负极 | |
| B. | pH=0.68时,反应处于平衡状态 | |
| C. | pH<0.68时,氧化性I2<AsO43- | |
| D. | pH=5时,负极电极反应式为2I--2e-=I2 |
16.已知:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1)△H1,
2CO(g)+O2(g)=2CO2(g)△H2
2H2(g)+O2(g)=2H2O(1)△H3;
2H2(g)+O2(g)=2H2O(g)△H4
CO(g)+2H2(g)=CH3OH(g)△H5
下列关于上述反应焓变的判断正确的是( )
2CO(g)+O2(g)=2CO2(g)△H2
2H2(g)+O2(g)=2H2O(1)△H3;
2H2(g)+O2(g)=2H2O(g)△H4
CO(g)+2H2(g)=CH3OH(g)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1<0,△H2>0 | B. | 0>△H3>△H4 | ||
| C. | 2△H5+△H1>0 | D. | △H1=△H2+△H3-2△H5 |
15.向含SO32-、Fe2+、Br-、I-各0.1mol的混合溶液中通入Cl2,Cl2与它们可能发生如下四个反应:①SO32-+Cl2+H2=SO42-+2Cl-+2H+,②2Fe2++Cl2=2Fe3++2Cl-,③2Br-+Cl2=Br2+2Cl-,④2I-+Cl2=I2+2Cl-.当通入0.2molCl2时,发生的反应是( )
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
14.若苯的环上三个氢原子分别被-Cl、-Br、-I取代,能生成的同分异构体数目是( )
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
13.短周期元素A、B、C、D、E原子序数依次增大,其中A、C同主族,B、E同主族,A的最外层电子数与次外层电子数相等,E是太阳能转化为电能的常用材料,则下列说法正确的是( )
| A. | 工业上用电解熔融氧化物的方法制备C单质 | |
| B. | 离子半径:C>D | |
| C. | 熔融它们的单质,所克服的微粒间作用力都相同 | |
| D. | 含D的盐溶液都显酸性 |
12.用下列实验装置进行相应实验,装置正确且能达到实验目的是( )


| A. | 用图a所示装置干燥NH3气体 | |
| B. | 用图b所示装置蒸发NaCl溶液得NaCl晶体 | |
| C. | 用图c所示装置分离有机层与水层,水层从分液漏斗下口放出 | |
| D. | 用图d所示装置测量氯气的体积 |
11.化学与材料、生活和环境密切相关.下列有关说法中正确的是( )
| A. | 侯氏制碱法是先将CO2通入饱和NaCl溶液后,再通入NH3 | |
| B. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 | |
| C. | PM2.5是指大气中直径≤2.5×10-6m的颗粒物(气溶胶),可通过加水吸收后再利用过滤的方法分离PM2.5微粒和可溶性吸附物 | |
| D. | “神十”航天服是由碳化硅陶瓷和碳纤维复合而制成的,它是一种新型无机非金属材料 |
8.下列物质的分类合理的是( )
0 155115 155123 155129 155133 155139 155141 155145 155151 155153 155159 155165 155169 155171 155175 155181 155183 155189 155193 155195 155199 155201 155205 155207 155209 155210 155211 155213 155214 155215 155217 155219 155223 155225 155229 155231 155235 155241 155243 155249 155253 155255 155259 155265 155271 155273 155279 155283 155285 155291 155295 155301 155309 203614
| A. | 碱性氧化物:Na2O、CaO、Al2O3、H2O | B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | ||
| C. | 氧化物:Fe2O3、NO、SO2、CuO | D. | 酸:H2SO4、HNO3、NaHSO4 |