1.A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中离子半径最小的,则它们的原子序数由小到大的顺序是( )
| A. | E、C、D、B、A | B. | B、A、E、D、C | C. | E、B、A、D、C | D. | A、B、C、D、E |
20.SO2在400~600℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中正确的是( )
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 通过调控反应条件,SO2可以100%地转化为SO3 | |
| C. | SO2的浓度与SO3的浓度相等时,反应达到平衡 | |
| D. | 因为反应放热,所以升高温度会使反应速率减慢 |
19.下列化学用语表达正确的是( )
| A. | 一氯甲烷的结构式CH3Cl | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 氯化铵的电子式 | D. | 苯的分子式 |
18.根据原子结构及元素周期律的知识,下列推断正确的是( )
| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 12C和石墨互为同素异形体 | |
| C. | Cl?、S2?、Ca2+、K+半径逐渐减小 | |
| D. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力相同 |
14.标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断正确的是( )
| A. | 原混合气体中CO与CH4的体积分数和为33.9% | |
| B. | 原混合气体中,C2H4与C2H2的体积共为1.9L | |
| C. | 反应完成后,生成水的质量为9g | |
| D. | 原混合气体中,CO与CH4的体积比一定为1:1 |
12.500mLKNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol•L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
0 155109 155117 155123 155127 155133 155135 155139 155145 155147 155153 155159 155163 155165 155169 155175 155177 155183 155187 155189 155193 155195 155199 155201 155203 155204 155205 155207 155208 155209 155211 155213 155217 155219 155223 155225 155229 155235 155237 155243 155247 155249 155253 155259 155265 155267 155273 155277 155279 155285 155289 155295 155303 203614
| A. | 原混合溶液中c(K+)为2mol•L-1 | B. | 上述电解过程中共转移2mol电子 | ||
| C. | 电解得到铜的物质的量为0.5mol | D. | 电解后溶液中c(H+)为2mol•L-1 |
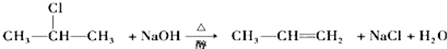
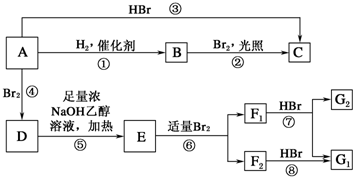
 ;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为
;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为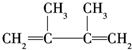 ;F1的结构简式为
;F1的结构简式为
 .
. .
. ;
;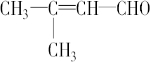 .
. 表示的分子式C7H12;名称是3-甲基-2,4-己二烯.
表示的分子式C7H12;名称是3-甲基-2,4-己二烯.