11.下列5个有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2=CHCOOH
②CH2=CHCOOCH3
③CH2=CHCH2OH
④CH3CH2CH2OH
⑤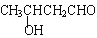
①CH2=CHCOOH
②CH2=CHCOOCH3
③CH2=CHCH2OH
④CH3CH2CH2OH
⑤
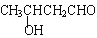
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
7.按下述实验方法制备气体,合理又实用的是( )
| A. | 锌粒与稀 HNO3反应制备 H2 | B. | 加热分解 NH4Cl 固体制 NH3 | ||
| C. | 大理石与稀 H2SO4反应制备 CO2 | D. | 亚硫酸钠与浓 H2SO4反应制备 SO2 |
6.短周期元素 W、X、Y 和Z的原子序数依次增大.W原子是半径最小的原子,非金属元素 X 形成的一种单质能导电,元素 Y 是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的 2 倍.下列说法错误的是( )
| A. | 元素 Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| B. | 元素 X与 W形成的共价化合物有很多种 | |
| C. | 元素 W、X的氯化物中,各原子均满足 8 电子的稳定结构 | |
| D. | 元素 Z 可与元素 X 形成共价化合物 XZ2 |
5.依据元素周期律可知同族元素所形成的同一类型的化合物,其结构和性质都相似.化合物 PH4I 是一种白色晶体,下列对它的描述中不正确的是( )
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为 PH3和 HI 或 H2和 I2 | |
| C. | 这种化合物能跟碱反应 | |
| D. | 该化合物可以由 PH3 和 HI 化合而成 |
4.一定温度下,在三个体积均为0.5L的恒容密闭容器中发生反应:CO(g)+Cl2(g)?C0Cl2(g),其中容器I中5min时到达平衡.下列说法中正确的是( )
| 温度/℃ | 起始物成质的量/mol | 平衡物质的两/mol | |||
| 容器编马 | CO | Cl2 | COCl2 | COCl2 | |
| Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
| Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
| Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 07 |
| A. | 容器I中前5min的平均反应速率v(CO)=0.16mol•L-1•min-1 | |
| B. | 该反应正反应为吸热反应 | |
| C. | 容器Ⅱ中起始时Cl2的物质的量为0.55mol | |
| D. | 若起始时向容器I加入CO0.8mol,Cl20.8mol,达到平衡时CO转化率大于80%. |
2.下列指定反应的离子方程式正确的是( )
0 155100 155108 155114 155118 155124 155126 155130 155136 155138 155144 155150 155154 155156 155160 155166 155168 155174 155178 155180 155184 155186 155190 155192 155194 155195 155196 155198 155199 155200 155202 155204 155208 155210 155214 155216 155220 155226 155228 155234 155238 155240 155244 155250 155256 155258 155264 155268 155270 155276 155280 155286 155294 203614
| A. | 向Ag(NH3)2NO3溶液中加人盐酸:Ag(NH3)++2H+═Ag++2NH4+ | |
| B. | 向 Na202 中加人足量水:2Na202+2H20═4Na++40H-+02↑ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++30H-═Al(0H)3↓ | |
| D. | 向 Ca(HC03)2溶液中加入澄淸石灰水:Ca2++2HC03-+20H-═CaC03↓+C032-+2H20 |

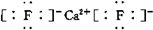 ;若 XY2其结构式为:S=C=S.为共价化合物时,
;若 XY2其结构式为:S=C=S.为共价化合物时,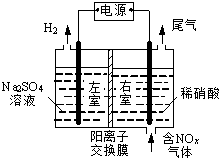 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).