5.表中有三组物质,每组都有一种物质与其他三种物质属于不同类别.请选出该物质,填在表相应的空格内.
| 序号 | 物质 | 被选出的 |
| (1) | O2、H2、C、N2 | C |
| (2) | Fe、Na、Al、Si | Si |
| (3) | NO、CO2、SO2、Fe3O4 | Fe3O4 |
4.下列各组物质中互为同分异构体的是( )
| A. | 葡萄糖和蔗糖 | B. | 蔗糖和麦芽糖 | ||
| C. | 甲酸甲酯(HCOOCH3)和乙酸(CH3COOH) | D. | 淀粉和纤维素 |
20.化学键的键能是指气态原子间形成1mol化学键时释放的能量.如:H(g)+I(g)→H-I(g)+297KJ即H-I键的键能为297KJ•mol-1,也可以理解为破坏1molH-I键需要吸收297KJ的热量.化学反应的发生可以看成旧化学键的破坏和新化学键的形成.下表是一些键能数据(单位:KJ•mol-1):
阅读上述信息,下列说法不正确的是( )
| 键能 | 键能 | 键能 | |||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 |
| S=S | 255 | H-S | 339 | C-F | 427 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
| C-O | 347 | H-O | 464 |
| A. | 键能越大,物质的热稳定性越强 | |
| B. | 热化学方程式H2(g)+Cl2(g)═2HCl(g);△H=-QkJ•mol-1中,Q的值为185 | |
| C. | H-O键的键能大于H-S键的键能,所以H2O的溶沸点高于H2S的溶沸点 | |
| D. | C-Br键的键能应在218kJ•mol-1-330kJ•mol-1之间 |
19.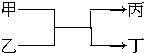 若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
 若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )| A. | 碳和镁 | B. | 氟气和氧气 | C. | 碳和氢气 | D. | 氧气和硫 |
18.为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验.下列说法正确的是( )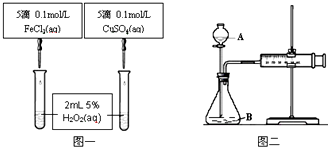

| A. | 图一可通过观察实验现象定量比较反应速率的大小 | |
| B. | 将CuSO4改为CuCl2更为合理 | |
| C. | 无法检查图二装置的气密性 | |
| D. | 图二所示实验中只需测量的数据是气体体积 |
17.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3NA | |
| B. | 标准状况下2.24L己烷分子中含有1.9NA对共用电子 | |
| C. | 0.1molFe与0.1mol氯气反应时失去的电子数为0.3NA | |
| D. | 电解精炼铜时,阳极质量每减少32g,电路中就转移NA个电子 |
16.化学在生产和生活中有着重要的作用.下列说法正确的是( )
0 155070 155078 155084 155088 155094 155096 155100 155106 155108 155114 155120 155124 155126 155130 155136 155138 155144 155148 155150 155154 155156 155160 155162 155164 155165 155166 155168 155169 155170 155172 155174 155178 155180 155184 155186 155190 155196 155198 155204 155208 155210 155214 155220 155226 155228 155234 155238 155240 155246 155250 155256 155264 203614
| A. | 茂密树林中的道道光柱,既谁一种自然现象又是光学现象,与胶体知识无关 | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| D. | CO2合成聚碳酸酯可降解塑料,以实现“碳”的循环利用 |
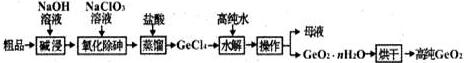
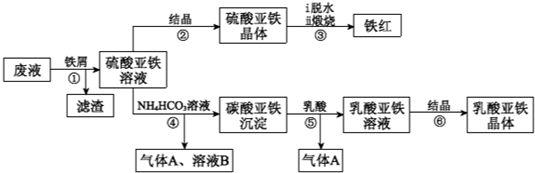
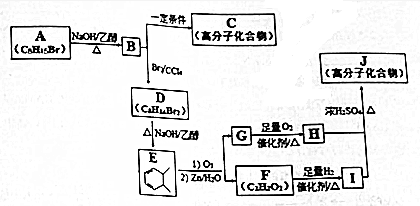
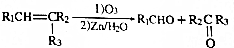
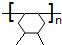 .
.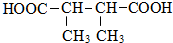 +n HOCH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2OH$→_{△}^{浓硫酸}$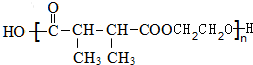 +(2n-1)H2O.
+(2n-1)H2O.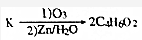 ,则K的同分异构体可能有7种(不考虑立体异构),写出其中一种的结构简式
,则K的同分异构体可能有7种(不考虑立体异构),写出其中一种的结构简式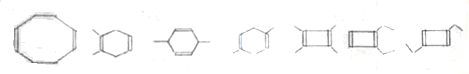 任意一种.
任意一种.