4.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
(1)写出实验中发生反应的离子方程式:Zn+2H+=Zn2++H2↑,该反应是放热反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
1.单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法不正确的是( )


| A. | 单斜硫和正交硫互为同素异形体 | |
| B. | 单斜硫比正交硫稳定 | |
| C. | 两种硫的燃烧反应均为放热反应 | |
| D. | S(s,单斜)=S(s,正交)△H=-0.33 kJ•mol-1 |
20.根据元素周期律的知识,下列两者性质比较中,正确的是( )
| A. | 热稳定性:HF<HCl | B. | 金属性强弱:K<Na | ||
| C. | 酸性强弱:H3PO4<H2SO4 | D. | 碱性强弱:NaOH<Mg(OH)2 |
19.下列所述的两者是同种物质的是( )
| A. | HCl和盐酸 | B. | 干冰和CO2 | C. | 正丁烷和异丁烷 | D. | 白磷和红磷 |
16.常温常压下,下列各组气体能共存的是( )
0 155064 155072 155078 155082 155088 155090 155094 155100 155102 155108 155114 155118 155120 155124 155130 155132 155138 155142 155144 155148 155150 155154 155156 155158 155159 155160 155162 155163 155164 155166 155168 155172 155174 155178 155180 155184 155190 155192 155198 155202 155204 155208 155214 155220 155222 155228 155232 155234 155240 155244 155250 155258 203614
| A. | SO2与O2 | B. | NO与O2 | C. | H2S与NO2 | D. | NH3和HCl |
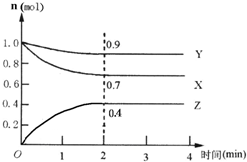 某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体).
某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体).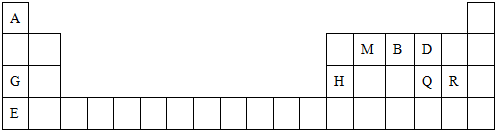
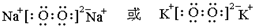 ;最高价氧化物的水化物中,酸性最强的化合物分子式为HClO4.
;最高价氧化物的水化物中,酸性最强的化合物分子式为HClO4.