5.硒为第四周期VIA族元素,根据它在周期表中位置推测,硒不可能具有的性质( )
| A. | 单质有还原性 | B. | 硒元素在化合物中可显-2价 | ||
| C. | 硒化氢水溶液显弱碱性 | D. | 最高价氧化物的水化物显酸性 |
4.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的元素符号可能是( )
| A. | N | B. | Ne | C. | P | D. | C |
3.下列说法中正确的是( )
| A. | 周期表中所有的族都是由长、短周期的元素共同组成 | |
| B. | 最外层电子数相同的元素不一定都是同一族 | |
| C. | 非金属元素都是主族元素,金属元素都是副族元素 | |
| D. | 元素周期表中共有18个纵行,每个纵行都是一个族,共有18个族 |
2.下列化学用语正确的是( )
| A. | 氯化氢的电子式  | B. | 镁的原子结构示意图: | ||
| C. | H2O和D2O是同素异形体 | D. | 40K和40Ca是同位素 |
1.下列反应属于吸热反应的是( )
| A. | 石灰石在高温下的分解反应 | B. | 铝热法炼铁 | ||
| C. | 实验室制氢气 | D. | 木炭在氧气中燃烧 |
20.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数c>d | B. | 非金属性Y<Z | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径W>X |
19.金属冶炼的实质是( )
| A. | 金属元素失去电子 | |
| B. | 金属元素获得电子 | |
| C. | 金属元素被氧化了 | |
| D. | 金属元素可能被氧化了,也可能被还原了 |
18.某化学小组以苯甲酸和异丙醇为原料,制取苯甲酸异丙酯(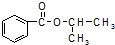 ),已知有关物质的沸点如表:
),已知有关物质的沸点如表:
合成苯甲酸异丙酯粗产品:
在如图圆底烧瓶中加入12.2g苯甲酸和30mL异丙醇(密度约为0.79g/cm3),再小心加入3mL浓硫酸,混匀后,加入几块碎瓷片,小心加热30分钟,使反应充分,得苯甲酸异丙酯粗产品.
(1)加入碎瓷片的目的是防止暴沸;
(2)异丙醇的系统命名法的名称为2-丙醇;
(3)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式 .
.
粗产品的精制:
(4)苯甲酸异丙酯粗产品中往往含有少量异丙醇、苯甲酸和水等,现拟用下列流程图进行精制,操作①中用到的一种重要玻璃仪器是分液漏斗;操作②的名称是蒸馏.
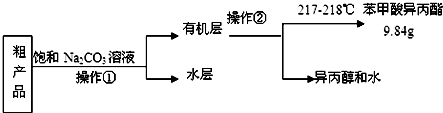
(5)结合上述相关数据进行计算,苯甲酸异丙酯的产率为60%.
(6)该实验中不能用下列那个选项所对应的措施来提高苯甲酸甲酯的产率A.
A.苯甲酸的质量由12.2g增加至24.4g
B.30ml的异丙醇增加至35mL.
0 155060 155068 155074 155078 155084 155086 155090 155096 155098 155104 155110 155114 155116 155120 155126 155128 155134 155138 155140 155144 155146 155150 155152 155154 155155 155156 155158 155159 155160 155162 155164 155168 155170 155174 155176 155180 155186 155188 155194 155198 155200 155204 155210 155216 155218 155224 155228 155230 155236 155240 155246 155254 203614
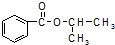 ),已知有关物质的沸点如表:
),已知有关物质的沸点如表:| 物质 | 异丙醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 82.4 | 249 | 218 |
在如图圆底烧瓶中加入12.2g苯甲酸和30mL异丙醇(密度约为0.79g/cm3),再小心加入3mL浓硫酸,混匀后,加入几块碎瓷片,小心加热30分钟,使反应充分,得苯甲酸异丙酯粗产品.
(1)加入碎瓷片的目的是防止暴沸;
(2)异丙醇的系统命名法的名称为2-丙醇;
(3)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式
 .
.粗产品的精制:
(4)苯甲酸异丙酯粗产品中往往含有少量异丙醇、苯甲酸和水等,现拟用下列流程图进行精制,操作①中用到的一种重要玻璃仪器是分液漏斗;操作②的名称是蒸馏.

(5)结合上述相关数据进行计算,苯甲酸异丙酯的产率为60%.
(6)该实验中不能用下列那个选项所对应的措施来提高苯甲酸甲酯的产率A.
A.苯甲酸的质量由12.2g增加至24.4g
B.30ml的异丙醇增加至35mL.
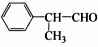 ,工业合成路线如下:
,工业合成路线如下: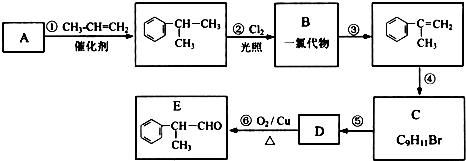
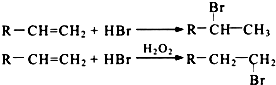 (R-代表烃基)
(R-代表烃基) 或
或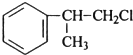 (任写一个),其官能团为氯原子.
(任写一个),其官能团为氯原子.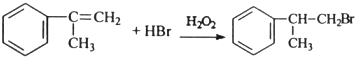 (必须有反应条件).
(必须有反应条件). .
.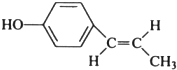 (只写反式结构).
(只写反式结构).