4.若在一定条件下,容积恒定的反应室中充入amolCO与2amolH2,在催化剂作用下发生反应CO(g)+2H2(g)?CH3OH(g),下列措施一定使$\frac{c(C{H}_{3}OH)}{c(CO)}$增大的是( )
| A. | 升高温度 | |
| B. | 恒温恒容再充入a mol CO和2a mol H2 | |
| C. | 恒温恒容再充入H2 | |
| D. | 充入Ar(g)使体系的总压增大 |
3.下列事实中,不能用勒夏特列原理解释的是( )
| A. | 冰镇的啤酒打开后泛起泡沫 | |
| B. | 对N2+3H2?2NH3的反应,使用铁触媒可加快合成氨反应的速率 | |
| C. | 工业制取金属钾Na(l)+KCl(l)?NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
2.下列有关说法正确的是( )
| A. | 工业上现在大规模采用电解熔融NaCl或AlCl3制取Na或Al | |
| B. | 若电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化 | |
| C. | 某反应的平衡常数K300℃>K350℃,则该反应△H<0 | |
| D. | 合成氨生产中将NH3液化分离,目的是加快正反应速率,提高H2的转化率 |
1.2015年巴黎气候变化大会召开,旨在保护环境造福人类.下列说法不正确的是( )
| A. | 采用碳捕集和储存技术,逐步实现二氧化碳的零排放 | |
| B. | 扩大铅蓄电池、汞锌锰等含重金属元素的干电池的生产,满足消费需求 | |
| C. | 对工业废水、生活污水净化处理,减少污染物的排放 | |
| D. | 催化处理汽车尾气,减轻氮氧化物污染和光化学烟雾 |
20.关于Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2+2H2O的下列说法中,正确得是( )
| A. | 氧化剂与还原剂的物质的量之比是2:1 | |
| B. | 当生成22.4LSO2气体时,转移的电子数目是2NA | |
| C. | 该反应写成离子式是Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$Cu+SO2↑+2H2O | |
| D. | 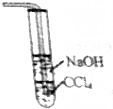 制备SO2装置尾气可用如图处理 |
17.化学与人类生活、社会可持续发展密切相关.下列说法正确的是( )
0 155054 155062 155068 155072 155078 155080 155084 155090 155092 155098 155104 155108 155110 155114 155120 155122 155128 155132 155134 155138 155140 155144 155146 155148 155149 155150 155152 155153 155154 155156 155158 155162 155164 155168 155170 155174 155180 155182 155188 155192 155194 155198 155204 155210 155212 155218 155222 155224 155230 155234 155240 155248 203614
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 用CO2合成聚碳酸酯可降解塑料,实现碳的循环利用 | |
| C. | “天宫一号”使用的碳纤维,是一种新型有机高分子材料 | |
| D. | 制作快餐饭盒的可降解“玉米塑料”(主要成分是聚乳酸)是纯净物 |

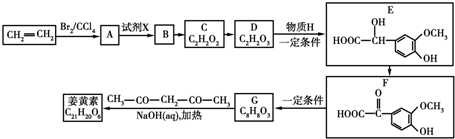


 .
.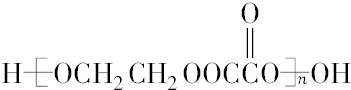 .
. .
. ;
; .
.