5. 常温下向25mL0.1mol•L-1 NaOH溶液中逐滴滴加0.2mol•L-1的HN3溶液(叠氮酸),pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7).下列说法正确的是( )
常温下向25mL0.1mol•L-1 NaOH溶液中逐滴滴加0.2mol•L-1的HN3溶液(叠氮酸),pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7).下列说法正确的是( )
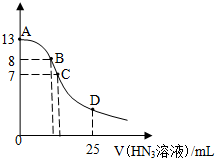
 常温下向25mL0.1mol•L-1 NaOH溶液中逐滴滴加0.2mol•L-1的HN3溶液(叠氮酸),pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7).下列说法正确的是( )
常温下向25mL0.1mol•L-1 NaOH溶液中逐滴滴加0.2mol•L-1的HN3溶液(叠氮酸),pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7).下列说法正确的是( )| A. | A点水电离出的c(H+)小于B点 | |
| B. | 在B点,离子浓度大小为 c(OH-)>c(H+)>c(Na+)>c(N3-) | |
| C. | 在C点,滴加的V(HN3)=12.5mL | |
| D. | 在D点,c(H+)≈10-4.7 |
3.下列说法正确的是( )
| A. | 在由水电离产生的氢离子浓度为10-13 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3-四种离子能大量共存 | |
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 | |
| C. | 对于反应2N2H4(l)=N2(g)+2H2(g),△H=-50.6 kJ?mol-1,它只在高温下自发进行 | |
| D. | 常温下,将0.2 mol?L-1某一元碱(ROH)溶液和0.1 mol?L-1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+) |
20.短周期元素A、B、C、D的原子序数依次增大.它们的原子序数之和为36,且原子的最外层电子数之和为14; A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D分别为同主族元素.下列叙述正确的是( )
| A. | 在地壳中,B元素的含量位于第二位 | |
| B. | C元素的单质熔点低,在空气中加热时先熔化后燃烧 | |
| C. | A、B、D三种元素形成的化合物一定是强酸 | |
| D. | B元素与A元素形成的物质一定是纯净物 |
18.短周期元素X、Y,X元素原子的最外层电子数与次外层电子数的差值等于电子层数;Y元素原子的最外层电子数比X元素原子的最外层电子数多2,则X与Y所形成的化合物的化学式为( )
| A. | X3Y2 | B. | X2Y | C. | X2Y5 | D. | XY3 |
17.X、Y、Z、W和N均是由短周期元素组成的五种化合物.已知五种化合物水溶液的焰色反应均呈黄色,Y、Z和N均由三种元素组成.请根据题目要求回答下列问题.
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有AC(填序号).
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)写出X与二氧化碳反应的化学方程式2CO2+2Na2O2═2Na2CO3+O2.
(3)下表为Y与Z实验的部分内容:
写出Y与稀硫酸反应的离子方程式S2O32-+2H+═S↓+SO2↑+H2O.
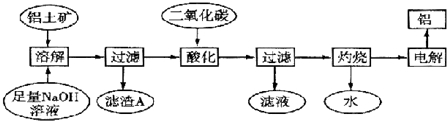
(4)写出含0.1mol Z的溶液与20mL 5mol•L-1的盐酸反应的离子反应式AlO2-+H++H2O═Al(OH)3↓.实验③加热蒸发、灼烧得到的最终产物主要是Al2O3.
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有AC(填序号).
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)写出X与二氧化碳反应的化学方程式2CO2+2Na2O2═2Na2CO3+O2.
(3)下表为Y与Z实验的部分内容:
| 序号 | 主要实验步骤及实验现象 |
| ① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
| ② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
(4)写出含0.1mol Z的溶液与20mL 5mol•L-1的盐酸反应的离子反应式AlO2-+H++H2O═Al(OH)3↓.实验③加热蒸发、灼烧得到的最终产物主要是Al2O3.
16.已知可逆反应:N(g)+M(g)?P(g)+Q(g)△H>0,请回答下列问题:
(1)若要增大M的转化率,在其他条件不变的情况下可以采取的措施为BC(填字母).
A.加入一定量M B.加入一定量N
C.将生成的气体P液化分离
D.缩小反应容器的体积
(2)不同温度下该反应的平衡常数如下:则K1< (填“>”或“<”)K2.
(3)某温度下,反应物的起始浓度[M]=1.0mol•L-1,[N]=2.4mol•L-1,达到平衡后,M的转化率为60%,此时N的转化率为25%,该反应的平衡常数Kc=0.5.
0 155044 155052 155058 155062 155068 155070 155074 155080 155082 155088 155094 155098 155100 155104 155110 155112 155118 155122 155124 155128 155130 155134 155136 155138 155139 155140 155142 155143 155144 155146 155148 155152 155154 155158 155160 155164 155170 155172 155178 155182 155184 155188 155194 155200 155202 155208 155212 155214 155220 155224 155230 155238 203614
(1)若要增大M的转化率,在其他条件不变的情况下可以采取的措施为BC(填字母).
A.加入一定量M B.加入一定量N
| 温度/℃ | 600 | 700 |
| 平衡常数 | K1 | K2 |
D.缩小反应容器的体积
(2)不同温度下该反应的平衡常数如下:则K1< (填“>”或“<”)K2.
(3)某温度下,反应物的起始浓度[M]=1.0mol•L-1,[N]=2.4mol•L-1,达到平衡后,M的转化率为60%,此时N的转化率为25%,该反应的平衡常数Kc=0.5.
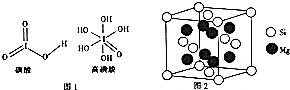 世界卫生组织(WHO)确认人体中的14种必需微量元素中有铜、铬、硅、碘、氟等.
世界卫生组织(WHO)确认人体中的14种必需微量元素中有铜、铬、硅、碘、氟等.