15.下列说法中正确的是( )
| A. | 核外电子排布完全相同的两种微粒,其化学性质一定相同 | |
| B. | 具有固定熔点或沸点的物质一定是纯净物 | |
| C. | 一种离子和一种分子的质子数和电子数不可能同时相等 | |
| D. | 由分子构成的物质中一定含有共价键 |
14.某同学将燃着的红磷放入装有氧气的集气瓶中燃烧,一段时间后,红磷熄灭,他立刻将燃烧匙取出,但此时红磷又开始燃烧.解释这种现象的说法错误的是( )
| A. | 红磷又接触到氧气 | |
| B. | 红磷的温度还高于它的着火点 | |
| C. | 燃烧时红磷转变成白磷,降低了着火点 | |
| D. | 瓶内的氧气不能耗尽红磷 |
13.硒是人体必须的微量元素,下列关于${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se的说法正确的是( )
| A. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se都含有34个中子 | |
| B. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se分别含有44和46个质子 | |
| C. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se因含有相同的质子数故互为同位素 | |
| D. | ${\;}_{34}^{78}$Se与${\;}_{34}^{80}$Se含有相同的电子数,因此性质一样 |
11.运用元素周期律分析,下列说法正确的是( )
| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素的最外层电子数等于元素的最高化合价 | |
| C. | 原子序数越大,原子半径越大 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
7.还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:
CrO42-$\underset{\stackrel{{H}^{+}}{→}}{转换}$Cr2O72-$\underset{\stackrel{F{e}^{2+}}{→}}{还原}$Cr3+$\underset{\stackrel{O{H}^{-}}{→}}{沉淀}$Cr(OH)3↓
已知转化过程中的反应为2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)
转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有$\frac{10}{11}$转化为Cr2072-,下列说法不正确的是( )
0 155043 155051 155057 155061 155067 155069 155073 155079 155081 155087 155093 155097 155099 155103 155109 155111 155117 155121 155123 155127 155129 155133 155135 155137 155138 155139 155141 155142 155143 155145 155147 155151 155153 155157 155159 155163 155169 155171 155177 155181 155183 155187 155193 155199 155201 155207 155211 155213 155219 155223 155229 155237 203614
CrO42-$\underset{\stackrel{{H}^{+}}{→}}{转换}$Cr2O72-$\underset{\stackrel{F{e}^{2+}}{→}}{还原}$Cr3+$\underset{\stackrel{O{H}^{-}}{→}}{沉淀}$Cr(OH)3↓
已知转化过程中的反应为2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)
转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有$\frac{10}{11}$转化为Cr2072-,下列说法不正确的是( )
| A. | 溶液颜色保持不变,说明上述可逆反应达到平衡状态 | |
| B. | 若用绿矾(FeS04•7H2O)作还原剂,处理1 L废水,至少需要458.7g | |
| C. | 常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5 | |
| D. | 常温下Ksp=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
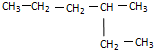 与
与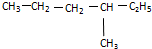 ⑨CS2
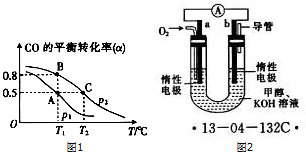
⑨CS2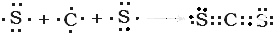 .
.
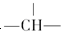 ,则该结构的烃的一氯取代物最多可能有几种(不考虑立体异构)( )
,则该结构的烃的一氯取代物最多可能有几种(不考虑立体异构)( )