5.在K2Cr2O7溶液中存在平衡:Cr2O72-(aq)+H2O(l)?2CrO42-(aq)+2H+(aq)
(橙色) (黄色)
下列说法正确的是( )
(橙色) (黄色)
下列说法正确的是( )
| A. | 滴加硫酸酸化的FeSO4溶液,平衡不移动 | |
| B. | 溶液颜色保持不变时,该反应达到平衡状态 | |
| C. | 滴加6 mol/L NaOH溶液,溶液颜色变深 | |
| D. | 平衡常数表达式为K=$\frac{2c(Cr{{O}_{4}}^{2-})•2c({H}^{+})}{c(C{r}_{2}{{O}_{7}}^{2-})•c({H}_{2}O)}$ |
1.在合成氨反应中,由a mol N2和b mol H2混合反应达到平衡时,有c mol NH3生成,则NH3在反应混合物中所占的体积分数是( )
0 155042 155050 155056 155060 155066 155068 155072 155078 155080 155086 155092 155096 155098 155102 155108 155110 155116 155120 155122 155126 155128 155132 155134 155136 155137 155138 155140 155141 155142 155144 155146 155150 155152 155156 155158 155162 155168 155170 155176 155180 155182 155186 155192 155198 155200 155206 155210 155212 155218 155222 155228 155236 203614
| A. | $\frac{100c}{a+b}$% | B. | $\frac{a}{a+b+c}$×100% | C. | $\frac{100c}{a+b-c}$% | D. | $\frac{100c}{a+b-\frac{c}{2}}$% |
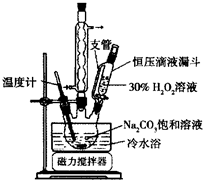 2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.
2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.
 H2O
H2O CO2
CO2 N2
N2 .
.