17.下列物质一定属于同系物的是( )
①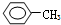
②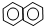
③
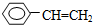
④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦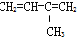
⑧
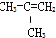
①

②
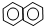
③
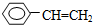
④C2H4
⑤CH2=CH-CH=CH2
⑥C3H6
⑦
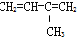
⑧
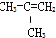
| A. | ④和⑥ | B. | ①、②和③ | C. | ⑤和⑦ | D. | ⑥和⑧ |
16.下列各组元素,按原子半径依次减小,元素第一电离能逐渐增大的顺序排列的是( )
| A. | K Na Li | B. | Al Mg Na | C. | N O C | D. | Cl S P |
15.关于电化学内容,下列说法正确的是( )
| A. | 氢氧燃料电池的负极反应式:O2+4H++4e-═2H2O | |
| B. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| C. | 粗铜精炼时,与电源正极相连是纯铜,电极反应式为Cu-2e-═Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
14.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g).平衡时测得 A 的浓度为0.50mol/L.保持温度不变,将容器的容积扩大到原来的两倍再达到平衡时,测得A的浓度为 0.30mol/L.下列判断正确的是( )
| A. | x+y>z | B. | 平衡向正反应方向移动 | ||
| C. | B 的转化率升高 | D. | C 的体积分数增加 |
13.在由水电离出的c(OH-)=1×10-13 mol/L的溶液中,可能大量共存的离子组是( )
| A. | Fe2+ Na+ NO3- Cl- | B. | Ba2+ Cu2+ NO${\;}_{3}^{-}$ Cl- | ||
| C. | SO42- SO3- NH4+ Na+ | D. | Mg2+ Na+ Br- ClO- |
12.在BaSO4饱和溶液中,加入Na2SO4(s),达平衡时( )
| A. | c(Ba2+)、c(SO42-)均增大 | |
| B. | c(Ba2+)=c(SO42-)=[Ksp(BaSO4)]1/2 | |
| C. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)=Ksp(BaSO4) | |
| D. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)≠Ksp(BaSO4) |
11.在2A(s)+B(g)?3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | v(A)=1.8 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=1.6 mol•L-1•s-1 |
8.硫酸性质是中学化学学习的重点.请回答下列问题:
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称:乙烯(写一种).
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验.
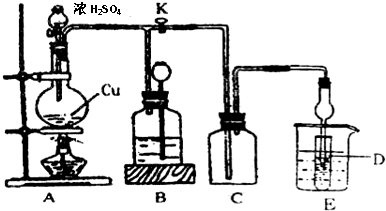
①装置B的作用是贮存多余的气体.B中应放置的液体是d(填序号).
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是b(填序号).
a.Fe粉b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是2Cu+2H2SO4+O2=2CuSO4+2H2O.
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是Ⅲ(填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为Cl2+SO2+2H2O=4H++2Cl-+SO42-.D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)=2 c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(3)利用FeCl3溶液的氧化性也可以吸收SO2.
①该反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.检验FeCl3是否完全被还原的方法为取少量反应后的溶液滴加少量硫氰化钾溶液,若不变红则氯化铁完全被还原.
②为验证FeCl3溶液与SO2的反应:同学们将SO2通入0.05mol•L-1 FeCl3溶液中,溶液很快由黄色变为红褐色; 将溶液长时间放置后,最终变为浅绿色. 关于红褐色液体,以下是同学们的分析推测及实验.
利用胶体的丁达尔效应(填性质) 可以检验步骤ⅰ中是否得到了Fe(OH) 3胶体.
根据反应b,说明步骤ⅱ中液体颜色变化的原因是加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应Fe3++6SO2?Fe(SO2)63+ 逆向移动(用离子方程式结合必要的文字说明).
0 155009 155017 155023 155027 155033 155035 155039 155045 155047 155053 155059 155063 155065 155069 155075 155077 155083 155087 155089 155093 155095 155099 155101 155103 155104 155105 155107 155108 155109 155111 155113 155117 155119 155123 155125 155129 155135 155137 155143 155147 155149 155153 155159 155165 155167 155173 155177 155179 155185 155189 155195 155203 203614
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称:乙烯(写一种).
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验.

①装置B的作用是贮存多余的气体.B中应放置的液体是d(填序号).
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是b(填序号).
a.Fe粉b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是2Cu+2H2SO4+O2=2CuSO4+2H2O.
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是Ⅲ(填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为Cl2+SO2+2H2O=4H++2Cl-+SO42-.D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)=2 c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(3)利用FeCl3溶液的氧化性也可以吸收SO2.
①该反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.检验FeCl3是否完全被还原的方法为取少量反应后的溶液滴加少量硫氰化钾溶液,若不变红则氯化铁完全被还原.
②为验证FeCl3溶液与SO2的反应:同学们将SO2通入0.05mol•L-1 FeCl3溶液中,溶液很快由黄色变为红褐色; 将溶液长时间放置后,最终变为浅绿色. 关于红褐色液体,以下是同学们的分析推测及实验.
| 分析推测 | 实验步骤及现象 |
| 甲:生成了Fe(OH) 3胶体 乙:经查阅资料,可能发生反应:Fe3++6SO2?Fe(SO2)63+ (反应b) | ⅰ.制备Fe(OH) 3胶体并检验 ⅱ.分别向Fe(OH) 3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
根据反应b,说明步骤ⅱ中液体颜色变化的原因是加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应Fe3++6SO2?Fe(SO2)63+ 逆向移动(用离子方程式结合必要的文字说明).