17.(1)CO2经过催化氢化可合成低碳烯烃.
其合成乙烯的反应为:2CO2(g)+6H2(g)?CH2=CH2(g)+4H2O(g);△H. 几种物质的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
则△H=-128kJ/mol
(2)以稀硫酸为电解质溶液,利用太阳能也可将CO2转化为低碳烯烃,工作原理图如图1.

①b电极的名称是正极.②产生丙烯的电极反应式为3CO2+18H++18e-=CH3CH=CH2+6H2O.
(3)工业上采用CO2与乙苯脱氢生产重要化工原料苯乙烯,反应如下:
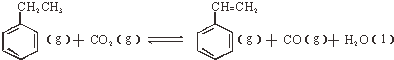 ;△H<0
;△H<0
①下列叙述能说明乙苯与CO2反应已达到平衡状态的是ad.
a.恒温恒压时气体密度不变b.c(CO2)=c(CO)
c.消耗1mol CO2同时生成 1mol H2O
d.CO2的体积分数保持不变
②在2L密闭容器内,CO2与乙苯发生反应.在三种不同的条件下进行实验,CO2、乙苯的起始浓度均分别为3mol/L和1mol/L,其中实验I在T1°C、P1 Pa下,而实验Ⅱ、Ⅲ分别改变了某一个实验条件(假设均不影响物质的状态),乙苯的浓度随时间的变化如图2所示.则:实验ⅠCO2在0-50min时的反应速率为0.012mol/(L•min).
实验Ⅲ可能改变的条件是升高温度.
③实验Ⅰ达到平衡后,在该温度下,向该容器中再通入CO2和乙苯各1mol,重新达到平衡时,乙苯的转化率将减少(填“增大”、“减小”或“不变”),此时平衡常数为0.375.
其合成乙烯的反应为:2CO2(g)+6H2(g)?CH2=CH2(g)+4H2O(g);△H. 几种物质的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
| 物质 | H2(g) | CO2(g) | CH2=CH2 | H2O(g) |
| 能量:KJ/mol | 0 | -394 | 52 | -242 |
(2)以稀硫酸为电解质溶液,利用太阳能也可将CO2转化为低碳烯烃,工作原理图如图1.

①b电极的名称是正极.②产生丙烯的电极反应式为3CO2+18H++18e-=CH3CH=CH2+6H2O.
(3)工业上采用CO2与乙苯脱氢生产重要化工原料苯乙烯,反应如下:
 ;△H<0
;△H<0①下列叙述能说明乙苯与CO2反应已达到平衡状态的是ad.
a.恒温恒压时气体密度不变b.c(CO2)=c(CO)
c.消耗1mol CO2同时生成 1mol H2O
d.CO2的体积分数保持不变
②在2L密闭容器内,CO2与乙苯发生反应.在三种不同的条件下进行实验,CO2、乙苯的起始浓度均分别为3mol/L和1mol/L,其中实验I在T1°C、P1 Pa下,而实验Ⅱ、Ⅲ分别改变了某一个实验条件(假设均不影响物质的状态),乙苯的浓度随时间的变化如图2所示.则:实验ⅠCO2在0-50min时的反应速率为0.012mol/(L•min).
实验Ⅲ可能改变的条件是升高温度.
③实验Ⅰ达到平衡后,在该温度下,向该容器中再通入CO2和乙苯各1mol,重新达到平衡时,乙苯的转化率将减少(填“增大”、“减小”或“不变”),此时平衡常数为0.375.
16.下列说法不正确的是( )
| A. | 发生爆炸的天津滨海仓库存放的电石、氰化钠和硝酸铵等危险化学品均属于电解质 | |
| B. | 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应 | |
| C. |  的系统命名为:2-甲基-2-乙基丙烷,其一氯代物有5种 的系统命名为:2-甲基-2-乙基丙烷,其一氯代物有5种 | |
| D. | 1mol化合物( )跟足量NaOH溶液反应最多耗4molNaOH )跟足量NaOH溶液反应最多耗4molNaOH |
15.下列反应的离子方程式书写正确的是( )
| A. | 98.3%的硫酸加入到稀氢氧化钡溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol | |
| B. | 向Ca(OH)2溶液中加入少量NaHCO3溶液产生白色沉淀:Ca2++2OH-+2HCO3-═CaCO3↓+CO3-+2H2O | |
| C. | 0.1mol/LNa2CO3溶液中滴入无色酚酞,溶液变红:CO32-+H2O═HCO3-+OH- | |
| D. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O |
14.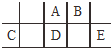 短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法不正确的是( )
短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法不正确的是( )
 短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法不正确的是( )
短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法不正确的是( )| A. | A有5种正价,与B可形成6种化合物 | |
| B. | 工业上常通过电解熔融态C2B3的方法来获得C的单质 | |
| C. | 简单离子的半径由大到小为:E>A>B>C | |
| D. | D、E两元素形成的化合物每种原子最外层都达到了8e-稳定结构 |
13.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 56gFe与1 molCl2充分反应转移电子数为3NA | |
| B. | 常温常压下,22 g D3O+含有10 NA个电子 | |
| C. | 25℃时,1 L pH=12的Ba(OH)2溶液中含有的OH-的数目为0.02 NA | |
| D. | 1 L0.1 mol/L Na2CO3溶液中CO32-和HCO3-总数为0.1NA |
12.我国古代人民编写的古诗或谚语包含了丰富的化学知识,下列解释正确的是( )
| 选项 | 古诗或谚语 | 含有的化学反应类型 |
| A | 爆竹声中除旧岁,春风送暖入屠苏 | 复分解反应 |
| B | 千锤万凿出深山,烈火焚烧若等闲 | 分解反应 |
| C | 春蚕到死丝方尽,蜡炬成灰泪始干 | 化合反应 |
| D | 真金不怕火,怕火便是铜 | 置换分解反应 |
| A. | A | B. | B | C. | C | D. | D |
11.化学与环境、生活密切相关,下列与化学有关的说法正确的是( )
| A. | 春节燃放爆竹对环境无污染 | |
| B. | “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 家庭用的“84”消毒液与洁厕灵可同时混合使用 |
10.通常把原子数和价电子数相同的分子或离子称为等电子体.人们发现等电子体的结构和性质相似.下列有关无机苯(B3N3H6)有关说法中错误的是( )
| A. | B3N3H6分子各原子均在同一平面上 | |
| B. | B3N3H6是由极性键组成的均匀而对称的非极性分子 | |
| C. | B3N3H6能发生加成反应和取代反应 | |
| D. | B3N3H6的二氯取代物有三种 |
9.下列有关晶体的叙述中,错误的是( )
| A. | 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 | |
| B. | 氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个 | |
| C. | 金属晶体中,铜和锌都是面心立方堆积 | |
| D. | 干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个 |
8.下列粒子属等电子体的是( )
0 155005 155013 155019 155023 155029 155031 155035 155041 155043 155049 155055 155059 155061 155065 155071 155073 155079 155083 155085 155089 155091 155095 155097 155099 155100 155101 155103 155104 155105 155107 155109 155113 155115 155119 155121 155125 155131 155133 155139 155143 155145 155149 155155 155161 155163 155169 155173 155175 155181 155185 155191 155199 203614
| A. | NO和O2 | B. | CH4和NH4+ | C. | N2H4和H2O2 | D. | HCl和H2O |