7.下列物质的分子中既有σ键,又有π键的是( )
| A. | HCl | B. | H2O | C. | H2O2 | D. | C2H2 |
6.下列分子中,所有原子都满足最外层为8电子结构的是( )
| A. | BF3 | B. | NCl3 | C. | PCl5 | D. | CHCl3 |
5.碳酸镍可用于电镀、陶瓷器着色等.镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS(含有Fe、Cu、Ca、Mg、Zn等元素杂质),从镍矿渣出发制备碳酸镍的流程如下:
已知:常温下,部分物质的溶度积常数如表:
(1)浸取过程中欲加快浸取速率,可采用的措施之一是将矿石粉碎(或提高浸取时的温度,或适当增大酸的浓度等合理答案均可);
(2)浸取出Ni2+时反应的离子方程式有①Ni(OH)2+2H+=Ni2++2H2O②NiS+ClO3-+H+→Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为1:3.
(3)加入Na2CO3溶液沉铁时生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6]和一种无色气体.写出此反应的离子方程式:3Fe3++3CO32-+Na++2SO42-+3H2O=NaFe3(SO4)2(OH)6+3CO2↑.
(4)加入NiS的作用是除去溶液中的Cu2+,反应的离子方程式为:Cu2++NiS=Ni2++CuS,过滤后,溶液中c(Ni2+)=0.107 mol•L-1时,溶液中残留c(Cu2+)为1.27×10-16mol•L-1.
(5)加入NaF的作用是除去Ca2+,有机萃取剂用于除去Zn2+.

已知:常温下,部分物质的溶度积常数如表:
难溶物 | NiS | ZnS | CuS | CaF2 | MgF2 |
| 溶度积常数 | 1.07×10-21 | 2.93×10-25 | 1.27×10-36 | 1.46×10-10 | 7.42×10-11 |
(2)浸取出Ni2+时反应的离子方程式有①Ni(OH)2+2H+=Ni2++2H2O②NiS+ClO3-+H+→Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为1:3.
(3)加入Na2CO3溶液沉铁时生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6]和一种无色气体.写出此反应的离子方程式:3Fe3++3CO32-+Na++2SO42-+3H2O=NaFe3(SO4)2(OH)6+3CO2↑.
(4)加入NiS的作用是除去溶液中的Cu2+,反应的离子方程式为:Cu2++NiS=Ni2++CuS,过滤后,溶液中c(Ni2+)=0.107 mol•L-1时,溶液中残留c(Cu2+)为1.27×10-16mol•L-1.
(5)加入NaF的作用是除去Ca2+,有机萃取剂用于除去Zn2+.
2.下列说法正确的是( )
| A. | 50℃时,测定某NaNO2溶液的pH=8,则溶液中c(Na+)-c(NO2-)=9.9×10-7mol•L-1 | |||||||||
| B. | NaHSO3水溶液中存在关系:c(H2SO3)+c(H+)=c(OH-)+c(SO32-)+c(HSO3-) | |||||||||
| C. | 一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| |||||||||
| D. | 已知25℃时,有关弱电解质的电离平衡常数:HCN:Ka=4.9×10-10;H2CO3:Ka1=4.3×10-7Ka2=5.6×10-11.则CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2=2HCN+Na2CO3 |
1.最近中美研究人员发明了一种可快速充电放电的铝离子电池,该电池电解质为离子液体,离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液,放电过程中不产生其他离子且有机阳离子不参与电极反应,放电时有关离子转化如图所示,下列说法正确的是( )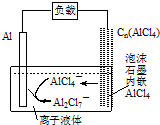

| A. | 放电时,负极发生:2AlCl4--e-=Al2Cl7-+Cl- | |
| B. | 放电时,电路中每流过3mol电子,正极减少27g | |
| C. | 充电时,泡沫石墨极与外电源的负极相连 | |
| D. | 充电时,阴极发生:4Al2Cl7-+3e-=Al+7AlCl4- |
20.下列说法不正确的是( )
| A. | 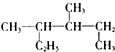 的系统命名是3,4-二甲基己烷 的系统命名是3,4-二甲基己烷 | |
| B. | 樱桃中含有一种羟基酸(如图所示)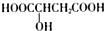 ,该羟基酸可以发生取代、氧化和缩聚等反应 ,该羟基酸可以发生取代、氧化和缩聚等反应 | |
| C. | 所有的糖、油脂、蛋白质都能水解,但水解产物不同 | |
| D. | 等质量的甲醛和乙酸充分燃烧耗氧量相同 |
19.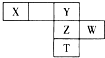 如图下表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X的最高正价与最低负价绝对值只差等于0.下列说法正确的是( )
如图下表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X的最高正价与最低负价绝对值只差等于0.下列说法正确的是( )
 如图下表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X的最高正价与最低负价绝对值只差等于0.下列说法正确的是( )
如图下表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X的最高正价与最低负价绝对值只差等于0.下列说法正确的是( )| A. | X氢化物的沸点一定比Y氢化物的沸点低 | |
| B. | T的最高价氧化物对应的水化物酸性比Z的强 | |
| C. | Y的氢化物沸点高于Z的氢化物,因为H-Y键的键能高于H-Z键 | |
| D. | XY2、XZ2、XW4的化学键类型相同、晶体类型也相同 |
18.下列说法正确的是( )
0 155004 155012 155018 155022 155028 155030 155034 155040 155042 155048 155054 155058 155060 155064 155070 155072 155078 155082 155084 155088 155090 155094 155096 155098 155099 155100 155102 155103 155104 155106 155108 155112 155114 155118 155120 155124 155130 155132 155138 155142 155144 155148 155154 155160 155162 155168 155172 155174 155180 155184 155190 155198 203614
| A. | 实验时皮肤受碱腐蚀,先用大量水冲洗,再用2%醋酸溶液或硼酸溶液洗,最后用水冲洗 | |
| B. | 萃取操作时,要快速振摇分液漏斗,放气时支管口不能对着人,也不能对着火 | |
| C. | 淀粉溶液中加入稀硫酸,加热后再加入适量银氨溶液,水浴加热,可以判断淀粉是否水解 | |
| D. | 液态溴乙烷中加入NaOH溶液共热几分钟,然后滴加AgNO3溶液,可以检验溴乙烷中含溴元素 |
 .
.
 .
. .
.