13.室温下,在pH=12的某溶液中,由水电离的c(OH-)可能为
①1.0×10-7 mol•L-1 ②1.0×10-6 mol•L-1 ③1.0×10-2 mol•L-1 ④1.0×10-12 mol•L-1.( )
①1.0×10-7 mol•L-1 ②1.0×10-6 mol•L-1 ③1.0×10-2 mol•L-1 ④1.0×10-12 mol•L-1.( )
| A. | ①④ | B. | ③② | C. | ④ | D. | ③④ |
11.下列物质属于离子化合物的是( )
| A. | HCl | B. | H2SO4 | C. | H2O | D. | CaCl2 |
10.已知短周期元素的离子 aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径:B>A>C>D | B. | 原子序数:d>c>b>a | ||
| C. | 离子半径:D ->C 2->B +>A 2+ | D. | 离子的还原性:D ->C 2- |
9.下列物质间的转化不能通过一步反应完成的是( )
| A. | SiO2→Si | B. | SiO2→H2SiO3 | C. | Si→Na2SiO3 | D. | CO2→C |
8.已知还原性I->Fe2+>Br-,下列离子方程式正确的是( )
| A. | 将少量Cl2通入FeBr2溶液中:Cl2+2Br-═Br2+2Cl- | |
| B. | 将足量Cl2通入FeBr2溶液中:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 将少量Cl2通入FeI2溶液中:2Fe2++2I-+3Cl2═2Fe3++2I2+6Cl- | |
| D. | 将672mLCl2(标况)通入250mL 0.1molL-1的FeI2溶液中:2Fe2++10I-+6Cl2═12Cl-+5I2+2Fe3+ |
7.Cu2O可用于制作船底防污漆,某学习小组探究制备Cu2O的方法.
【查阅资料】
①CuSO4与Na2SO3溶液混合可制备Cu2O.
②Cu2O为砖红色固体;酸性条件下生成Cu2+和Cu.
③Cu2O和Cu(SO3)23-可以相互转化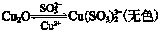
(1)配制0.25mol•L-1CuSO4溶液和0.25mol•L-1 Na2SO3溶液.测得CuSO4溶液pH=4,Na2SO3溶液pH=9.用离子方程式表示CuSO4溶液pH=4的原因Cu2++2H2O?Cu(OH)2+2H+.
(2)完成CuSO4溶液和Na2SO3溶液反应制Cu2O的离子方程式:
□Cu2++□SO32-+□2H2O $\frac{\underline{\;\;△\;\;}}{\;}$□Cu2O↓+□SO42-+□HSO3-
【实验探究】
(3)证明 ii中砖红色沉淀是Cu2O的实验方案是取少量砖红色沉淀于试管中,加入稀硫酸,溶液变为蓝色,说明砖红色沉淀是Cu2O.
(4)经检验 i中黄色沉淀含有Cu2SO3,ii中沉淀由黄色变砖红色的化学方程式是Cu2SO3═Cu2O+SO2↑.
(5)iii中砖红色沉淀消失的原因是Cu2O转化得无色Cu(SO3)23-.
(6)在加热条件下,若向2mL 0.25mol•L-1Na2SO3溶液中滴加0.25mol•L-1CuSO4溶液至
过量,预期观察到的现象是产生砖红色沉淀,且沉淀不消失.
(7)由上述实验得出结论:CuSO4溶液和Na2SO3溶液反应制备Cu2O,应控制的条件是
反应温度、CuSO4和Na2SO3的物质的量之比.
【查阅资料】
①CuSO4与Na2SO3溶液混合可制备Cu2O.
②Cu2O为砖红色固体;酸性条件下生成Cu2+和Cu.
③Cu2O和Cu(SO3)23-可以相互转化
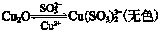
(1)配制0.25mol•L-1CuSO4溶液和0.25mol•L-1 Na2SO3溶液.测得CuSO4溶液pH=4,Na2SO3溶液pH=9.用离子方程式表示CuSO4溶液pH=4的原因Cu2++2H2O?Cu(OH)2+2H+.
(2)完成CuSO4溶液和Na2SO3溶液反应制Cu2O的离子方程式:
□Cu2++□SO32-+□2H2O $\frac{\underline{\;\;△\;\;}}{\;}$□Cu2O↓+□SO42-+□HSO3-
【实验探究】
| 操作 | 现象 |
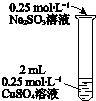 | i 有黄色沉淀出现,随着 Na2SO3溶液的滴入,沉淀增加,当加到5mL时,溶液的蓝色消失. ii 将试管加热,黄色沉淀变为砖红色,有刺激性气味气体产生. iii在加热条件下,继续滴入Na2SO3溶液,砖红色沉淀减少,当1加到10mL时,沉淀完全溶解,得无色溶液. |
(4)经检验 i中黄色沉淀含有Cu2SO3,ii中沉淀由黄色变砖红色的化学方程式是Cu2SO3═Cu2O+SO2↑.
(5)iii中砖红色沉淀消失的原因是Cu2O转化得无色Cu(SO3)23-.
(6)在加热条件下,若向2mL 0.25mol•L-1Na2SO3溶液中滴加0.25mol•L-1CuSO4溶液至
过量,预期观察到的现象是产生砖红色沉淀,且沉淀不消失.
(7)由上述实验得出结论:CuSO4溶液和Na2SO3溶液反应制备Cu2O,应控制的条件是
反应温度、CuSO4和Na2SO3的物质的量之比.
4.下列有关化学反应中能量变化的理解,正确的是( )
0 154987 154995 155001 155005 155011 155013 155017 155023 155025 155031 155037 155041 155043 155047 155053 155055 155061 155065 155067 155071 155073 155077 155079 155081 155082 155083 155085 155086 155087 155089 155091 155095 155097 155101 155103 155107 155113 155115 155121 155125 155127 155131 155137 155143 155145 155151 155155 155157 155163 155167 155173 155181 203614
| A. | 需要加热才能发生的反应,一定是吸收能量的反应 | |
| B. | 在化学反应过程中总是伴随着能量的变化 | |
| C. | 释放能量的反应在常温下一定很容易发生 | |
| D. | 在确定的化学反应中反应物的总能量总是高于生成物的总能量 |